Questão 69985
UCS 2016
(Ucs 2016) O 1,2 - dicloroetano ocupa posição de destaque na indústria química americana. Trata-se de um líquido oleoso e incolor, de odor forte, inflamável e altamente tóxico. É empregado na produção do cloreto de vinila que, por sua vez, é utilizado na produção do PVC, matéria-prima para a fabricação de dutos e tubos rígidos para água e esgoto.
A equação química que descreve, simplificadamente, o processo de obtenção industrial do 1,2 - dicloroetano a partir da reação de adição de gás cloro ao eteno, encontra-se representada abaixo.
Disponível em: <http://laboratorios.cetesb.sp.gov.br/wp-content/uploads/sites/47/2013/11/dicloroetano.pdf>. Acesso em: 3 set. 15. (Adaptado.)
Dados:
| Ligação | Energia de ligação |
| C - H | 413,4 |
| C - Cl | 327,2 |
| C - C | 346,8 |
| C = C | 614,2 |
| Cl - Cl | 242,6 |
A variação de entalpia da reação acima é igual a
-144,4 kJ/mol
-230,6 kJ/mol
-363,8 kJ/mol
+428,2 kJ/mol
+445,0 kJ/mol
Gabarito:
-144,4 kJ/mol
Resolução:
Equação da reação representada com as fórmulas estruturais
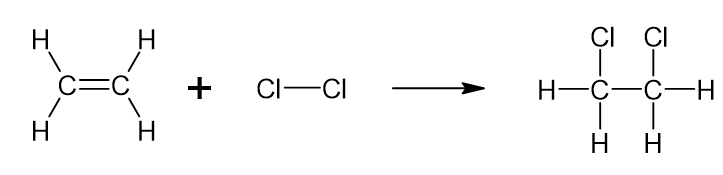
Nessa reação ocorre a formação de uma ligação C-C, duas ligações C-Cl e quatro ligações C-H e a quebra de uma ligação C=C, uma ligação Cl-Cl e quatro ligações C-H.
A quebra de ligações é endotérmica e a formação de ligações é exotérmica, então a entalpia da reação pode ser calculada em termos das entalpias das ligações a partir da equação
Substituição dos valores