Questão 7
IME 2008
(IME - 2008/2009)
Considere a proposta de um processo para a obtenção da cementita, esquematizada abaixo.
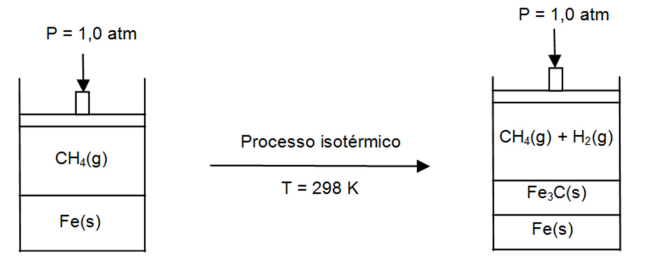
Sabe-se que a energia livre de Gibbs molar está relacionada diretamente com a constante de equilíbrio de uma reação química, conforme a seguinte equação termodinâmica:
Determine as frações molares na fase gasosa, na situação de equilíbrio, e avalie se o processo é viável.
Dados:

Gabarito:
Resolução:
Equação balanceada da reação:
3 Fe(s) + CH4(g) ⇌ Fe3C(s) + 2 H2(g)
A energia de Gibbs pode ser calculada pela equação
ΔGº = ΔHº - TΔSº
• Cálculo da entalpia padrão de reação:
ΔHºr = (ΔHºf Fe3C + 2 x ΔHºf H2) - (ΔHºf CH4 + 3 ΔHºf Fe)
ΔHºr = (25,10 + 0 ) - (0 - 74,80)
ΔHºr = 99,90 kJ.mol-1
• Cálculo da entropia padrão de reação:
ΔSºr = (ΔSºf Fe3C + 2 x ΔSºf H2) - (ΔSºf CH4 + 3 ΔSºf Fe)
ΔSºr = (104,6 + 2 x 130,6 ) - (186,2 - 3 x 27,30)
ΔSºr = 97,7 J.mol-1K-1
• Cálculo da energia livrede Gibbs padrão de reação:
ΔGº = ΔHº - TΔSº
ΔGº = 99,90 x 103 J.mol-1 - 298K x 97,7 J.mol-1K-1
ΔGº = 70,79 kJ.mol-1
• Cálculo da constante de equilíbrio em função das pressões parciais (Kp):
ΔGº = -RT lnKp
lnKp = - ΔGº/RT
lnKp = - 70,79 x 103 / 8,314 x 298
lnKp = -28,57
e, portanto
Kp = 3,91 x 10-13
A constante de equilíbrio em função das pressões parciais é definida como a razão entre as pressões parciais dos gases dos produtos pelas pressões parciais dos gases dos reagente elevados aos seus respectivos coeficientes estequiométricos:
Kp = pH22 / pCH4
Analisando a tabela de equilíbrio
| 3 Fe(s) | + CH4(g) | ⇌ | Fe3C(s) | + 2 H2(g) | |
| início | 1 atm | 0 | |||
| reage | x | 2x | |||
| equilíbrio | 1 - x | 2x |
Pode-se escrever a expressão
Kp = 4x2 / (1-x)
Como Kp é muito pequeno, x também é um muito pequeno e pode-se aproximar 1-x ≈ 1. Portanto:
Kp = 4x2
3,91 x 10-13 = 4x2
x = 3,13 x 10-7 atm
A pressão parcial de H2 é 2x. Portanto:
pH2 = 2x = 6,16 x 10-7 atm
A pressão parcial de CH4 é aproximadamente 1 atm. A pressão parcial e a quantidade de matéria são proporcionais, então pode-se calcular a fração molar em termos das pressões parciais:
Xi = pi / ptotal
Portanto, a fração molar de H2 é
XH2 = 6,16 x 10-7 / 1
XH2 = 6,16 x 10-7
e
XCH4 ≈ 1
Como a constante de equilíbrio tem um valor muito baixo, o processo não é viável.