Questão 5
ENEM 2018
(ENEM - 2018)
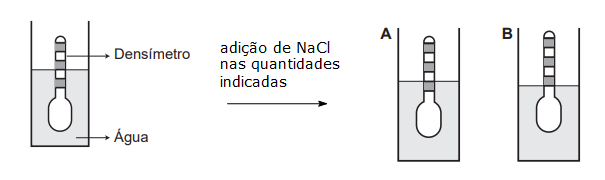
Usando um densímetro cuja maior divisão da escala isto é, a diferença entre duas marcações consecutivas, é de 5,0 x 10-2 g cm-3, um estudante realizou um teste de densidade: colocou este instrumento na água pura e observou que ele atingiu o repouso na posição mostrada.
Em dois outros recipientes A e B contendo 2 litros água pura, em cada um, ele adicionou 100 g e 200 g de NaCl, respectivamente.
Quando o cloreto de sódio é adicionado à água pura ocorre sua dissociação formando os íons Na+ e Cl-. Considere que esses íons ocupam os espaços intermoleculares na solução.
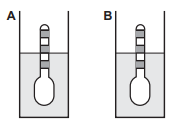
Nestes recipientes, a posição de equilíbrio do densímetro está representada em:
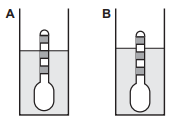
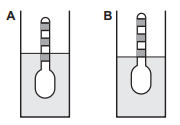
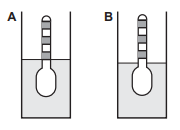
Gabarito:

Resolução:
A densidade é definida como a massa da solução dividida pelo volume da solução:
• Solução A: 2000cm3 de água + 100g de NaCl
A massa da solução A é a soma da massa da água e a massa de NaCl adicionada (2000g + 100g).
O volume da solução A é o volume de água (2000cm3)
• Solução B: 2000cm3 de água + 200g de NaCl
A massa da solução B é a soma da massa da água e a massa de NaCl adicionada (2000g + 200g).
O volume da solução B é o volume de água (2000cm3)
O densímetro sobe uma marcação para cada 0,05g.cm-3 na diferença entre a densidade da solução e a densidade da água pura. A densidade da água é 1,00g.cm-3.
A diferença entre a densidade da solução A e da água pura é de 0,05g.cm-3, então o densímetro sobe uma marcação.
A diferença entre a densidade da solução B e da água pura é de 0,10g.cm-3, então o densímetro sobe duas marcações.
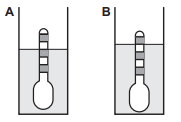
A alternativa que melhor representa essa descrição é a alternativa D: