Questão 52
UNESP 2022
(UNESP - 2022 - 2ª FASE) Em um recipiente de paredes rígidas, estão confinados 4 mols de um gás monoatômico ideal que, ao absorver determinada quantidade de calor, sofreu uma transformação isovolumétrica entre dois estados, I e II, representada no diagrama P × V.
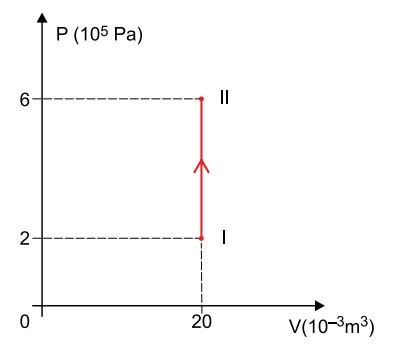
Adotando os valores para a constante universal dos gases e
para o calor específico molar desse gás a volume constante, a quantidade de calor absorvida pelo gás para que sofresse tal transformação foi de
16000 J.
14000 J.
18000 J.
12000 J.
10000 J.
Gabarito:
12000 J.
Resolução:
Observando o gráfico, é possível notar que do estado I ao estado II, o volume se manteve constante, logo a transformação é isocórica.
Neste caso, o trabalho da força de pressão do gás é nulo e, de acordo com a primeira lei da Termodinâmica, a variação de energia interna se deve às trocas de calor entre o gás e o meio.
equação 1
Como temos um gás monoatômico e ideal, a variação de energia interna é dada por:
Sabemos que , substituindo na equação 1
Mas
Então: