Questão 79
UNESP 2022
(UNESP - 2022 - 1ª fase - DIA 2)
Em um experimento de calorimetria realizado no nível do mar, um estudante colocou 600 g de água a 10 ºC e 100 g de gelo a –40 ºC em um calorímetro ideal, onde já existiam 800 g de água a 5 ºC, em equilíbrio térmico com o calorímetro.
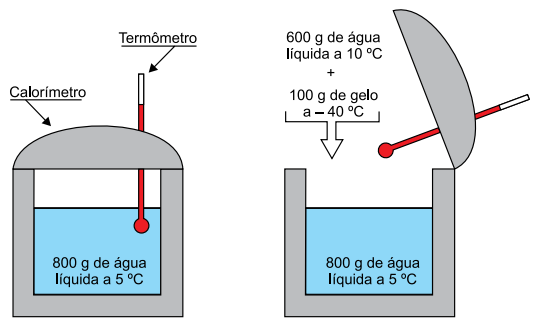
Sabendo que o calor específico da água líquida é 1 cal/(g·ºC), que o calor específico do gelo é 0,5 cal/(g·ºC) e que o calor latente de fusão do gelo é 80 cal/g, depois de atingido o novo equilíbrio térmico havia, dentro do calorímetro,
1500 g de água líquida a 10 ºC.
1450 g de água líquida e 50 g de gelo a 0 ºC.
1500 g de gelo a –5 ºC.
1500 g de água líquida a 0 ºC.
1500 g de gelo a 0 ºC.
Gabarito:
1500 g de água líquida a 0 ºC.
Resolução:
Para a situação descrita, temos três componentes em diferentes temperaturas:
I). água líquida a 10º C :
m = 600 g e c = 1 cal/g.ºC
Q = 600.10 = - 6000 cal
II) gelo a -40ºC :
m = 100 g e c = 0.5 cal/g.ºC
Para 'esquentar' o gelo até 0ºC precisaríamos :
Q = 100.0,5.40 = 2000 cal
E para fundir todo o gelo Q = mL
Q = 100.80 = 8000 cal
III) Água líquida n calorímetro a 5ºC:
m = 800 g e c= 1 cal/g.ºC
Q = 800.1.-5 = -4000 cal
Somando-se todas as calorias Q = 2000 + 8000 - 4000 - 6000 = 0
Portanto, todo o gelo se fundiu e a água encontra-se líquida a 0ºC, sendo a massa total de água:
Q = 100 + 800 + 600 = 1500 g