Questão 33
UFPR 2015
(UFPR - 2015 - 1ª FASE)
Um cilindro com dilatação térmica desprezível possui volume de 25 litros. Nele estava contido um gás sob pressão de 4 atmosferas e temperatura de 227oC. Uma válvula de controle do gás do cilindro foi aberta até que a pressão no cilindro fosse de 1 atm. Verificou-se que, nessa situação, a temperatura do gás e do cilindro era a ambiente e igual a 27oC.
(Considere que a temperatura de 0oC corresponde a 273 K)
Assinale a alternativa que apresenta o volume de gás que escapou do cilindro, em litros.
11,8.
35.
60.
85.
241.
Gabarito:
35.
Resolução:
Gases são altamente expansíveis e compressíveis. Dessa forma, variar a pressão e temperatura de um gás pode aumentar ou diminuir seu volume. O que aconteceu é que antes o gás estava altamente comprimido com uma pressão de 4 atmosferas. Logo em seguida, foi aberta uma válvula que permitiu o escape do gás e assim o gás escapou até que a pressão no cilindro fosse de 1 atm. Um gás sempre ocupa todo o volume de seu recipiente, portanto o gás que sobrou dentro do cilíndro expandiu-se e reesfriou. Observe o diagrama:
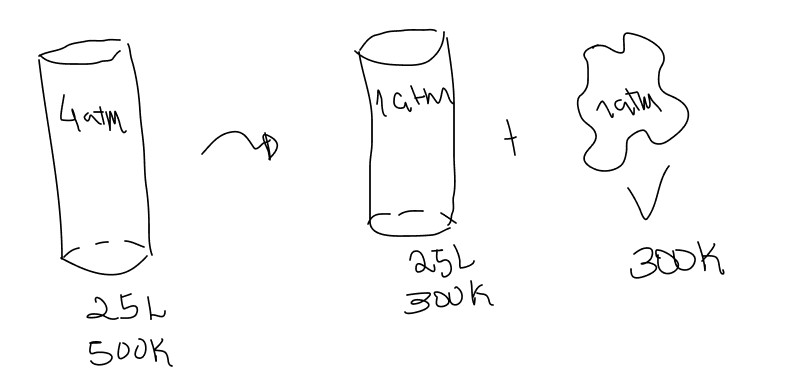
Portanto, podemos equacionar: