Questão 68509
UFG 2013
(UFG - 2013)
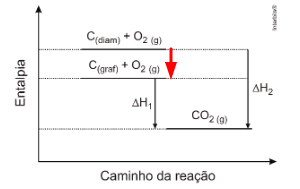
A alotropia dos elementos químicos afeta a entalpia da reação. Duas das formas alotrópicas do carbono são o grafite e o diamante. Observe o diagrama de entalpia a seguir.
Dados:
ΔH1 = -393,1 kJ/mol
ΔH2 = -395,0 kJ/mol
Ante o exposto, conclui-se que a conversão de diamante em grafite envolve
absorção de 1,9 kJ/mol.
liberação de 1,9 kJ/mol.
absorção de 788 kJ/mol.
liberação de 788 kJ/mol
absorção de 395 kJ/mol.
Gabarito:
liberação de 1,9 kJ/mol.
Resolução:
ΔH1 = -393,1 kJ/mol
ΔH2 = -395,0 kJ/mol
ΔH2 = ΔH1 + ΔHvermelho
-395,0 = -393,1 + ΔHvermelho
ΔHvermelho = -395,0 - (-393,1)
ΔHvermelho = -395,0 + 393,1
ΔHvermelho = 1,9
Como o sinal é negativo, ocorre liberação da energia.