Questão 60
ITA 2023
(ITA - 2023 - 1ª FASE)
Os seguintes diagramas representam diferentes estados de equilíbrio de uma reação exotérmica do tipo
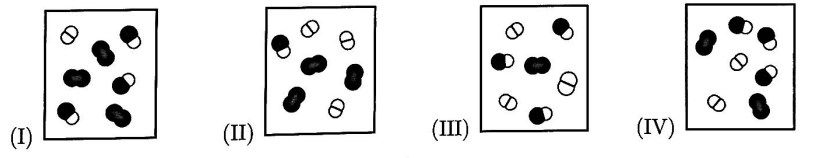
Assinale a opção que contém a afirmação CORRETA.
Se a constante de equilíbrio da reação, KC, em uma determinada temperatura, é igual a 3, apenas o diagrama (I) representa o sistema no equilíbrio.
Os diagramas (II) e (IV) podem representar a situação da reação em equilíbrio em duas temperaturas diferentes, com TII > TIV.
Se todos os diagramas representam a reação em equilíbrio, o diagrama (III) representa a reação com a menor constante de equilíbrio.
Se a pressão for reduzida à metade pela duplicação do volume, em temperatura constante, os diagramas (II) e (III) representam a reação em equilíbrio para estado inicial e final, respectivamente, desse processo, com VII = 2VIII.
Se cada símbolo que representa uma molécula nos diagramas equivale a 0,20 mol e se o volume do recipiente é 1,0 L, a constante de equilíbrio da reação representada pelo diagrama (I) é 0,5.
Gabarito:
Os diagramas (II) e (IV) podem representar a situação da reação em equilíbrio em duas temperaturas diferentes, com TII > TIV.
Resolução:
A) FALSO.
Analisando os sitemas:
Sistema 1:
Sistema 2:
Sistema 3:
Sistema 4:
Sistema 1 e 3 apresentariam equilíbrio para .
B) VERDADEIRO.
A reação por ser exotérmica, com o aumento da temperatura, há um deslocamento do equilíbrio para os reagentes. Assim, II possui mais reagentes que IV.
C) FALSO.
Como calculado acima, o sistema 2 possui a menor constante de equilíbrio.
D) FALSO.
Como na reação não há variação de volume, a pressão não desloca o equilíbrio.
E) FALSO.
Para o sistema 1, teríamos:
.