Questão 4
ITA 2011
(ITA 2011 - 2ª fase)
A reação química hipotética representada pela seguinte equação: foi acompanhada experimentalmente, medindo-se as concentrações das espécies [AB2C], [AB2] e [C2] em função do tempo. A partir destas informações experimentais, foram determinadas a constante de velocidade e a lei de velocidade da reação (k). Com base nessa lei de velocidade, o mecanismo abaixo foi proposto e aceito
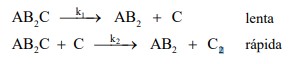
Explique como foi possível determinar a constante de velocidade (k).
Gabarito:
Resolução:
Lei de velocidade da etapa lenta:
A velocidade pode ser reescrita como a taxa de variação da concentração de [AB2C] com o tempo t
Integral de t0 a t e [AB2C]0 a [AB2C]:
se t0 = 0
Se a concentração de AB2C for metade da concentração inicial, o tempo t é igual ao tempo de meia vida:
Conhecendo a quantidade inicial de AB2C e monitorando o tempo da reação, é possível determinar o tempo de meia vida e, portanto, a constante de velocidade k1.