Questão 2
ITA 2011
(ITA - 2011 - 1ª Fase)
Assinale a opção que apresenta o ácido mais forte, considerando que todos se encontram nas mesmas condições de concentração, temperatura e pressão.
CH3COOH
CH3CH2COOH
(CH3)3CCOOH
CℓCH2COOH
Cℓ3CCOOH
Gabarito:
Cℓ3CCOOH
Resolução:
A força de um ácido está relacionada à facilidade de ionizar liberando H+, portanto, quanto mais enfraquecida for a ligação O-H, maior a acidez. Entre as alternativas, deve-se encontrar a ligação mais fraca, lembrando que grupos doadores de densidade eletrônica fortalecem a ligação O-H e grupos retiradores enfraquecem a ligação.
Comparando o efeito indutivo das espécies das alternativas:
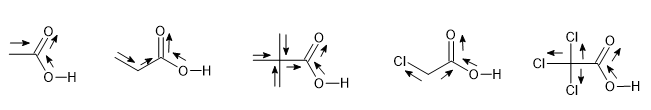
Como o item [E] tem a maior quantidade de grupos retiradores de densidade eletrônica, vai ter a ligação mais enfraquecida, facilitando a liberação de H+, aumentando o caráter ácido da espécie.
Gabarito: alternativa E