Questão 19
ITA 2010
[ITA 2010 - 1 FASE]
Considere duas reações químicas, mantidas à temperatura e pressão ambientes, descritas pelas equações abaixo:
I. H2(g) + ½ O2(g) H2O(g)
II. H2(g) + ½ O2(g) H2O(
)
Assinale a opção que apresenta a afirmação ERRADA sobre estas reações.
Gabarito:
Na reação I, o valor, em módulo, da variação de entalpia é menor que o da variação de energia interna.
Resolução:
Reações I e II (exotérmicas):
I) H2(g) + ½ O2(g) → H2O(g) ∆HI < 0
∆UI < 0
II) H2(g) + ½ O2(g) → H2O(l) ∆HII < 0
∆UII < 0

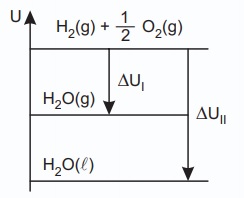
∆H (variação de entalpia) //// ∆U (variação de energia interna):
∆H = ∆U + ∆ngás R T
reação I: ∆ngás = – 0,5 mol
∆HI = ∆UI – 0,5 RT
Sendo assim a capacidade calorífica da H2O(l) (1cal/g°C) é maior que da H2O(g) (0,48 cal/g°C).
Gabarito B.