Questão 1
ITA 2010
(ITA - 2010 - 2ª Fase)
Determine o valor aproximado do pH no ponto de equivalência, quando se titula 25,0 mL de ácido acético 0,1000 mol·L-1 com hidróxido de sódio 0,1000 mol·L-1.
Sabe-se que log 2 = 0,3 e Ka = 1,8 x 10–5.
Gabarito:
Resolução:
A reação que ocorre entre o ácido acético e o hidróxido de sódio é representada pela equação:
H3CCOOH + NaOH → H3CCOONa + H2O
A quantidade de matéria adicionada de ácido acético foi de:
0,1000 mol de H3CCOOH ----------- 1000 mL
x -------------------------------------------- 25 mL
x = 2,5x10-3 mol de H3CCOOH
No ponto de equivalência, a quantidade de matéria de ácido e base se igualam, portanto, nH3CCOOH = nNaOH, sendo assim, a quantidade de matéia de base também será 2,5x10-3 mol.
O volume utilizado de base para garantir que foram adicionados 2,5x10-3 mol, sabendo que a concentração da solução de NaOH é 0,1000 mol·L-1 é:
0,1000 mol de NaOH -------------- 1000 mL
2,5x10-3 mol de NaOH ----------- y
y = 25 mL da solução de NaOH
No ponto de equivalência, o volume total da solução é 50 mL, sendo 25 mL da solução ácida e 25mL da solução básica. Portanto, é possível afirmar que a concentração de ácido acético é:
Sendo o ácido acético um ácido fraco, o H3CCOONa irá sofre hidrólise segundo a reação:
H3CCOONa + H2O → H3CCOOH + Na+ + OH-
H3CCOO- + H2O → H3CCOOH + OH-
Para calcular o pH da solução final é preciso saber qual a concentração de OH- após a hidrólise, para isso:
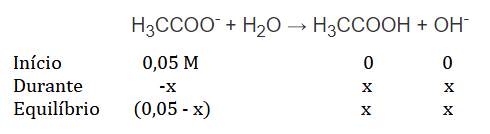
Sendo assim, a constante de hidrólise é:
Como x é pode ser desprezado perante 0,05:
A constante de hidrólise se relaciona com Ka da seguinte maneira:
Sendo: Kw = 10-14 ; Ka = 1,8x10-5.
Como "x" é igual a [OH-], pode-se afirmar que [OH-] = 5,27x10-6 mol/L.
Para finalizar e encontrar o valor de pH, é necessário encontrar a concentração de H+ a partir dos dados calculados. Para isso:
O pH é calculado por:
O pH da solução na ponto de equivalência é aproximadamente 8,7.