Questão 37
IME 2007
(IME - 2007/2008) Para a reação genérica aA → bB + cC, analise os cinco casos abaixo.
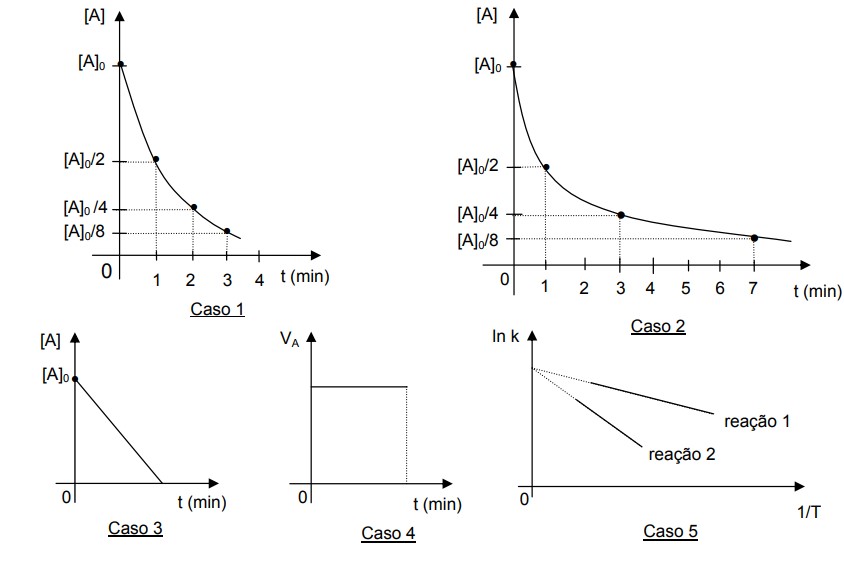
Considere que [A]0 = concentração molar inicial de A; VA = velocidade de reação; ki = constante de velocidade no i-ésimo caso; Ea = energia de ativação; e T = temperatura absoluta. A partir das informações contidas nos gráficos, assinale a alternativa correta.
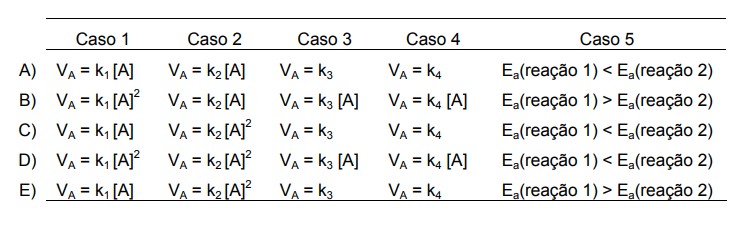
A
B
C
D
E
Gabarito:
C
Resolução:
Caso 1- A curva da concentração em função do tempo é uma exponencial. Ela representa uma reação de primeira ordem. Junto ao decaimento radioativo, temos um tempo de meia vida. Os pontos da curva podem ser representados por:
[A]=[A]0
A função característica do decaimento de primeira ordem é:
[A]=[A]0 e-k1t
Como T1/2 = 1 min, segue que k1 =ln2 min-1.
Dessa forma, por ser uma reação de primeira ordem, VA=k1[A].
Caso 2 - A curva da concentração em função do tempo é uma hipérbole. Assim, sabemos que se trata de uma reação de segunda ordem. Os pontos dessa curva podem ser representados por:
Neste caso temos k2 = 1/[A]0 min-1
Sendo uma reação de segunda ordem, VA=k2[A]2
Caso 3 e Caso 4 – A variação da concentração em função do tempo é constante velocidade constante. As duas são curvas características de uma reação de ordem zero. Assim VA=k3 e VA=k4
Caso 5 - Segundo a equação de Arrhenius:
A constante de velocidade pode ser escrita como:
k=Ae-Ea/Rt
onde
A: constante de Arrhenius
Ea: energia de ativação
R: constante universal dos gases.
Linearizando a equação temos
cuja inclinação(coeficiente angular) é representada por -Ea/R. Dessa forma, a curva mais inclinada apresenta maior energia de ativação.
Portanto, Letra C.