Questão 33
ESPCEX 2013
(EsPCEx - 2013)
Baseado no texto a seguir responda à(s) questão(ões).
Reações conhecidas pelo nome de Termita são comumente utilizadas em granadas incendiárias para destruição de artefatos, como peças de morteiro, por atingir temperaturas altíssimas devido à intensa quantidade de calor liberada e por produzir ferro metálico na alma das peças, inutilizando-as. Uma reação de Termita muito comum envolve a mistura entre alumínio metálico e óxido de ferro III, na proporção adequada, e gera como produtos o ferro metálico e o óxido de alumínio, além de calor, conforme mostra a equação da reação:

Dados:
Massas atômicas: Aℓ = 27 u; Fe = 56 u e O = 16 u
Entalpia Padrão de Formação:
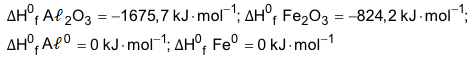
Considerando que para a inutilização de uma peça de morteiro seja necessária à produção de 336 g de ferro metálico na alma da peça e admitindo-se o alumínio como reagente limitante e o rendimento da reação de 100% em relação ao alumínio, a proporção em porcentagem de massa de alumínio metálico que deve compor 900 g da mistura de termita supracitada (alumínio metálico e óxido de ferro III) numa granada incendiária, visando à inutilização desta peça de morteiro, é de
3%
18%
32%
43%
56%
Gabarito:
18%
Resolução:
A reação do enunciado é:
Temos, então, que o consumo de alumínio é diretamente proporcional a formação do ferro (1:1). O enunciado diz que será formado 336 gramas de ferro metálico e que o alumínio é o limitante da reação. Podemos encontrar a massa de alumínio consumido:
1 mol de Al __________ 1 mol de Fe
27 gramas de Al ______ 56 gramas de Fe
x gramas ____________ 336 gramas de Fe
x = 162 gramas
Logo, em 900 gramas da mistura de termita, teremos 162 gramas de alumínio. Em porcentagem, isso equivale a:
900 gramas _______ 100%
162 gramas _______ y
y = 18%