Questão 63521
ALBERT EINSTEIN 2016
(Fac. Albert Einstein 2016)
O gráfico a seguir representa a pressão de vapor de quatro solventes em função da temperatura.
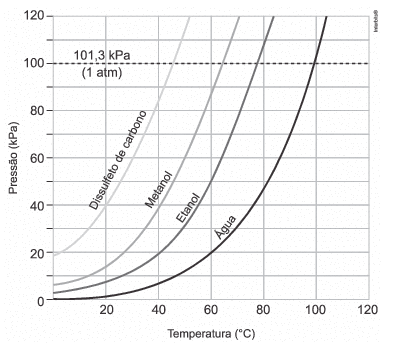
Ao analisar o gráfico foram feitas as seguintes observações:
I. Apesar de metanol e etanol apresentarem ligações de hidrogênio entre suas moléculas, o etanol tem maior temperatura de ebulição, pois sua massa molecular é maior do que a do metanol.
II. É possível ferver a água a 60 °C, caso essa substância esteja submetida uma pressão de 20 kPa.
III. Pode-se encontrar o dissulfeto de carbono no estado líquido a 50 °C, caso esteja submetido a uma pressão de 120 kPa.
Pode-se afirmar que
somente as afirmações I e II estão corretas.
somente as afirmações I e III estão corretas.
somente as afirmações II e III estão corretas.
todas as afirmações estão corretas.
Gabarito:
todas as afirmações estão corretas.
Resolução:
I. Correta. Apesar de metanol e etanol apresentarem ligações de hidrogênio entre suas moléculas, o etanol tem maior temperatura de ebulição, pois sua massa molecular é maior do que a do metanol.
Para os monoalcoóis alifáticos saturados, à medida que aumenta a massa molecular, a temperatura de ebulição aumenta.
II. Correta. É possível ferver a água a 60 °C, caso essa substância esteja submetida uma pressão de 20 kPa.
Na pressão de 20 kPa, a temperatura de ebulição da água é 60°C (vide gráfico).
III. Correta. Pode-se encontrar o dissulfeto de carbono no estado líquido a 50 °C, caso esteja submetido a uma pressão de 120 kPa.
Sob pressão de 120 kPa, a temperatura de ebulição do dissulfeto de carbono é um pouco maior que 50°C (Te > 50°C). Logo, na temperatura de 50°C, o dissulfeto de carbono encontra-se no estado líquido.