Questão 133
ENEM 2020
(ENEM PPL - 2020)
Os tanques de armazenamento de gasolina podem, com o tempo, sofrer processos oxidativos, resultando na contaminação do combustível e do solo à sua volta. Uma forma de evitar tais problemas econômicos e ambientais é utilizar preferencialmente metais de sacrifício, protegendo os tanques de armazenamento.
Suponha que seja necessário usar um metal de sacrifício em um tanque de aço (liga de ferro-carbono). Considere as semirreações de redução e seus respectivos potenciais padrão.
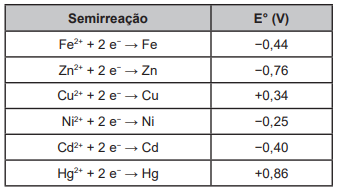
Dos metais citados, o que garantirá proteção ao tanque de aço é o
zinco.
cobre.
níquel.
cádmio.
mercúrio.
Gabarito:
zinco.
Resolução:
A tabela nos dá a informação do potencial de redução dos metais apresentados. Como o tanque é feito de uma liga de aço que tem em sua composição ferro, vamos analisar o potencial desse metal.
A situação problema da questão nos diz que os tanques estão sofrendo oxidação e, consequentemente, contaminando o combustível armazenado e o solo em sua volta. Como o potencial de oxidação é o valor contrário ao potencial de redução, temos que:
Fe → Fe2+ + 2e- Eº = +0,44 V
Os metais de sacrifício são utilizados com o intuito de protegerem o material da oxidação. Para isso, procuramos o metal que tenha um potencial de oxidação maior do que o do ferro. Esse metal irá se oxidar primeiro do que o ferro, por ter um potencial maior para isso, por isso o nome sacrifício. Pela tabela, o único que terá potencial de oxidação maior será o Zinco:
Zn → Zn2+ + 2e- Eº = +0,76 V