Questão 126
ENEM 2020
(ENEM PPL - 2020)
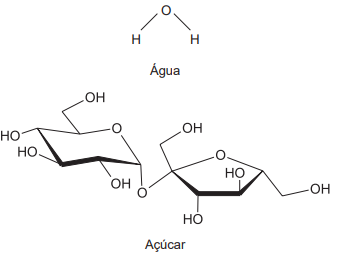
Um princípio importante na dissolução de solutos é que semelhante dissolve semelhante. Isso explica, por exemplo, o açúcar se dissolver em grandes quantidades na água, ao passo que o óleo não se dissolve.
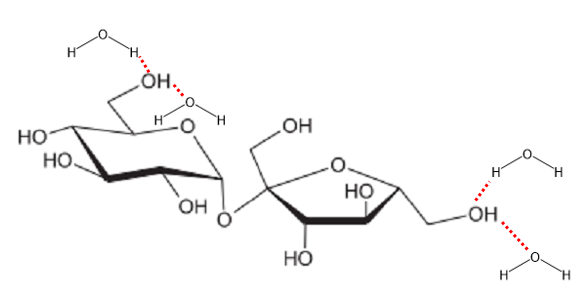
A dissolução na água, do soluto apresentado, ocorre predominantemente por meio da formação de
ligações iônicas.
ligações covalentes.
interações íon-dipolo.
ligações de hidrogênio.
interações hidrofóbicas.
Gabarito:
ligações de hidrogênio.
Resolução:
Como diz o enunciado, semelhante dissolve semelhante. A molécula de água e da sacarose (açúcar) são polares, enquanto que o óleo é composto por moléculas apolares e não se dissolve em água.
A dissolução da sacarose na água se da, predominantemente, pelas ligações de hidrogênios que as moléculas do solvente realizam com as hidroxilas do soluto. As ligações de hidrogênio são interações intermoleculares (entre as moléculas) onde o hidrogênio de uma molécula ligado à um átomo de Flúor, Oxigênio ou Nitrogênio recebe o par de elétrons de um átomo de outra molécula (normalmente, um átomo de Flúor, Oxigênio ou Nitrogênio).