Questão 114
ENEM 2020
(ENEM PPL - 2020)
O peróxido de hidrogênio é um produto secundário do metabolismo celular e apresenta algumas funções úteis, mas, quando em excesso, é prejudicial, gerando radicais que são tóxicos para as células. Para se defender, o organismo vivo utiliza a enzima catalase, que decompõe em
e
. A energia de reação de decomposição, quando na presença e ausência da catalase, está mostrada no gráfico.
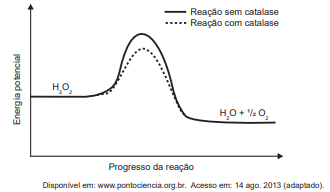
Na situação descrita, o organismo utiliza a catalase porque ela
diminui a energia de ativação
permite maior rendimento da reação.
diminui o valor da entalpia da reação.
consome rapidamente o oxigênio do reagente.
reage rapidamente com o peróxido de hidrogênio.
Gabarito:
diminui a energia de ativação
Resolução:
a) [correta] diminui a energia de ativação
Podemos ver no gráfico que a energia de ativação da reação com catalase é menor.
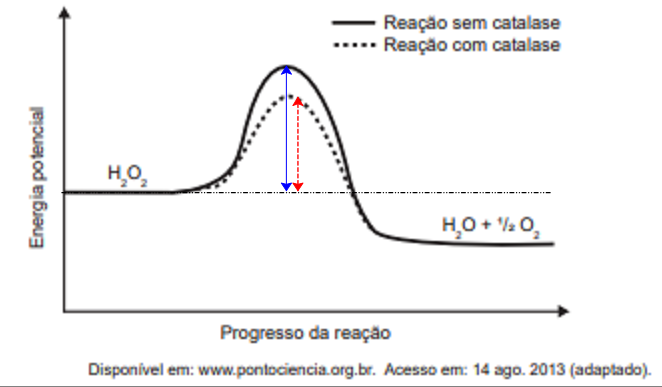
b) [errada] permite maior rendimento da reação.
O rendimento da reação não é influenciado pela catalase.
c) [errada] diminui o valor da entalpia da reação.
Podemos ver no gráfico que a variação de entalpia da reação permanece o mesmo.
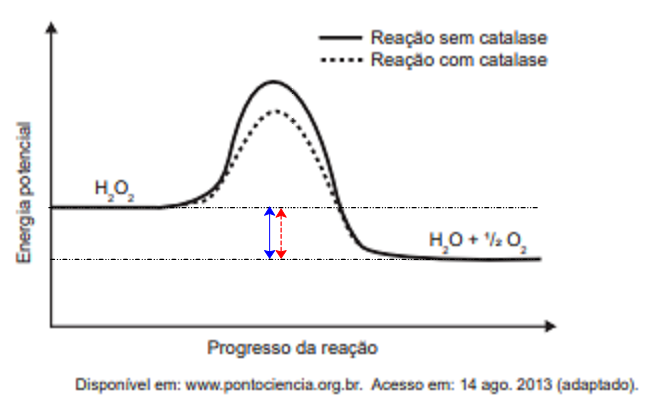
d) [errada] consome rapidamente o oxigênio do reagente.
A catalase não vai consumir o oxigênio, apenas acelerar o processo reacional do H2O2
e) [errada] reage rapidamente com o peróxido de hidrogênio.
A catalase não vai reagir com o H2O2, apenas acelerar sua decomposição em H2O e O2