Questão 93
ENEM 2020
(ENEM PPL - 2020)
A água sofre transições de fase sem que ocorra variação da pressão externa. A figura representa a ocorrência dessas transições em um laboratório.
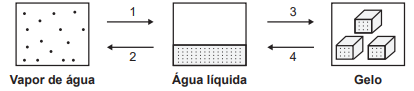
Tendo como base as transições de fase representadas (1 a 4), a quantidade de energia absorvida na etapa 2 é igual à quantidade de energia
liberada na etapa 4.
absorvida na etapa 3.
liberada na etapa 3.
absorvida na etapa 1.
liberada na etapa 1.
Gabarito:
liberada na etapa 1.
Resolução:
O estado vapor possui mais energia que o estado sólido. Logo, para transformar vapor de água para água líquida, é necessário que seja liberada energia, em forma de calor. Esse processo é exotérmico e se repete do estado líquido para o gasoso. Seguindo essa lógica, o sólido, que tem pouca energia, necessita ganhar calor para que se transforme em líquido, um processo endotérmico.
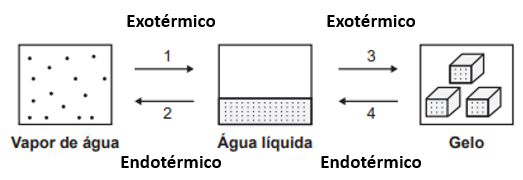
O processo 2 é um processo endotérmico, a água irá receber energia em forma de calor para chegar ao estado vapor. Como a energia gasta para que o vapor se torne líquido deve se conservar, o processo que terá energia igual ao processo 2 deve ser o processo 1.