Questão 16
UNICAMP 2014
(UNICAMP - 2014)
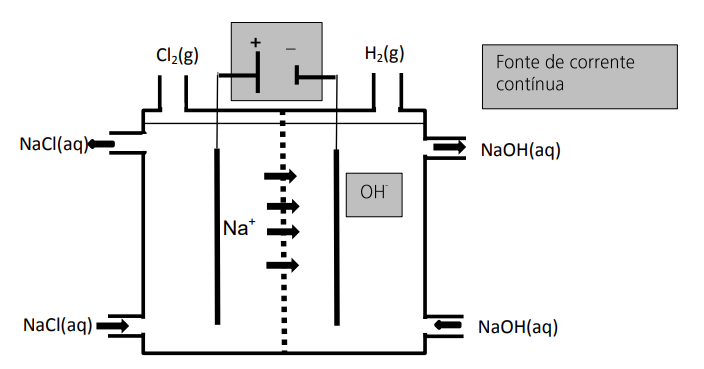
A produção mundial de gás cloro é de 60 milhões de toneladas por ano. Um processo eletroquímico moderno e menos agressivo ao meio ambiente, em que se utiliza uma membrana semipermeável, evita que toneladas de mercúrio, utilizado no processo eletroquímico convencional, sejam dispensadas anualmente na natureza. Esse processo moderno está parcialmente esquematizado na figura abaixo.
a) Se a produção anual de gás cloro fosse obtida apenas pelo processo esquematizado na figura abaixo, qual seria a produção de gás hidrogênio em milhões de toneladas?
b) Na figura, falta representar uma fonte de corrente elétrica e a formação de íons OH- . Complete o desenho com essas informações, não se esquecendo de anotar os sinais da fonte e de indicar se ela é uma fonte de corrente alternada ou de corrente contínua.
Gabarito:
Resolução:
a) Equação da reação de eletrólise do NaCl:
2 H2O + 2 NaCl → H2 + Cl2 + OH-
A proporção em quantidade de matéria de Cl2 e H2 é de 1:1. Como a massa molar do gás cloro é 71 g/mol e a massa molar do gás hidrogênio é 2 g/mol, a massa de gás hidrogênio produzida considerando a obtenção anual de 60 milhões de toneladas de gás cloro é
| 71 g Cl2 | __________ | 2 g H2 |
| 60 x 106 ton | __________ | m |
A massa de gás hidrogênio produzida é 1,69 milhões de toneladas.
b)