Questão 59795
UERJ 2006
"Na natureza nada se cria, nada se perde; tudo se transforma."
Esse enunciado é conhecido como Lei da Conservação das Massas ou Lei de Lavoisier. Na época em que foi formulado, sua validadae foi contestada, já que na queima de diferentes substâncias era possível observar o aumento ou diminuição de massa.
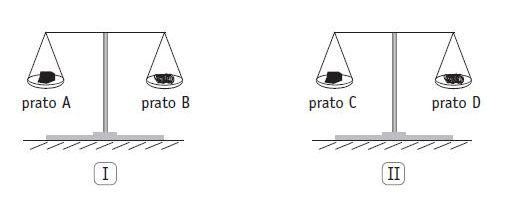
Para exemplificar esse fenômeno, considere as duas balanças idênticas I e II mostradas na figura a seguir. Nos pratos dessas balanças foram colocadas massas idênticas de carvão e de esponja de aço, assim distribuídas:
- pratos A e C: carvão;
- pratos B e D: esponja de aço.
A seguir, nas mesmas condições reacionais, foram queimados os materiais contidos em B e C, o que provocou desequilíbrio nos pratos das balanças. Para reestabelecer o equilíbrio, serão necessários procedimentos de adição e retirada de massas, respectivamente, nos seguintes pratos:
A e D
B e C
C e A
D e B
Gabarito:
A e D
Resolução:
- pratos A e C: carvão;
- pratos B e D: esponja de aço.
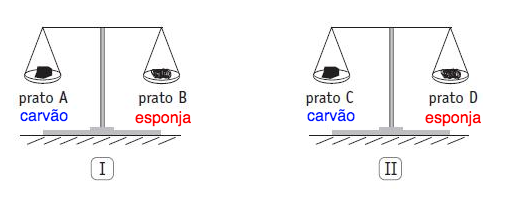
A queima da esponja de aço (B) se dá pela seguinte reação:
4Fe(s) + 2O2(g) → 2Fe2O3(s)
Parte da massa do produto vem do O2 que se encontrava no estado gasoso, e com isso na balança, o prato B vai ter maior massa que anteriormente.
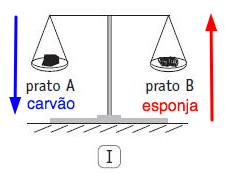
A queima do carvão (C) se dá pela seguinte reação:
C(s) + O2(g) → CO2(g)
Aqui temos toda a massa, inclusive do sólido presente na balança, se tornando um composto gasoso, fazendo com que a massa em C seja menor que anteriormente.
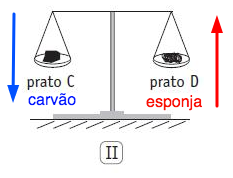
Para se reestabelecer o equilíbrio em I, devemos:
Retirar a massa extra formada em B ou adicionar a massa perdida de A.
Para se reestabelecer o equilíbrio em II, devemos:
Retirar a massa extra em D ou adicionar a massa perdida de C.
Gabarito alternativa A.