Questão 29699
PUC 2013
O dicromato de potássio (K2Cr2O7) pode ser utilizado para a determinação do teor de carbono orgânico do solo. A reação não balanceada está representada a seguir:
Sobre esse processo foram feitas algumas afirmações:
I. O ânion dicromato é o agente oxidante, possibilitando a oxidação da matéria orgânica a dióxido de carbono.
II. É necessário 0,5 L de solução aquosa de dicromato de concentração 0,20 mol·L-1 para oxidar completamente, em meio ácido, 4,50 g de matéria orgânica presente no solo.
III. Na reação para cada mol de dicromato (Cr2O7-2) que reage são consumidos 8 mol de cátions H+.
Sobre essas sentenças pode-se afirmar que
apenas a I é verdadeira.
apenas a II é verdadeira.
apenas a I e a III são verdadeiras.
apenas a II e a III são verdadeiras.
todas são verdadeiras.
Gabarito:
todas são verdadeiras.
Resolução:
O primeiro passo para resolver essa questão é fazer o balanceamento. Para isso será utilizada o método por oxirredução.
• Analisando o nox dos elementos:
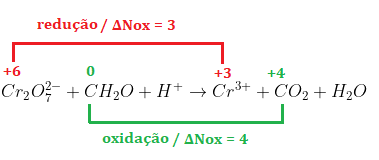
• Invertendo o nox da redução e da oxidação e associando como coeficiente estequiométrico:

• Substituindo esses valores na equação:
4 Cr2O7-2 + 6 CH2O + H+ → Cr3+ + CO2 + H2O
• Prosseguindo com o balanceamento por tentativa:
» 8 átomos de cromo nos reagentes e 1 nos produtos ⇒ multiplica o Cr+3 por 8.
4 Cr2O7-2 + 6 CH2O + H+ → 8 Cr3+ + CO2 + H2O
» 6 átomos de carbono nos reagentes e 1 nos produtos ⇒ multiplica o CO2 por 6.
4 Cr2O7-2 + 6 CH2O + H+ → 8 Cr3+ + 6 CO2 + H2O
» 34 átomos de oxigênio nos reagentes e 12 nos produtos ⇒ multiplica o H2O por 22.
4 Cr2O7-2 + 6 CH2O + H+ → 8 Cr3+ + 6 CO2 + 22 H2O
» 44 átomos de hidrogênio nos produtos e 13 nos reagentes ⇒ multiplica o H+ por 32.
4 Cr2O7-2 + 6 CH2O + 32 H+ → 8 Cr3+ + 6 CO2 + 22 H2O
» Dividindo todas as espécies por 2 para chegar nos menores valores inteiros:
2 Cr2O7-2 + 3 CH2O + 16 H+ → 4 Cr3+ + 3 CO2 + 11 H2O
Analisando cada uma das afirmativas:
I. O ânion dicromato é o agente oxidante, possibilitando a oxidação da matéria orgânica a dióxido de carbono.
Correta. O ânion dicromato (Cr2O7-2) reduz, portanto é o agente oxidante.
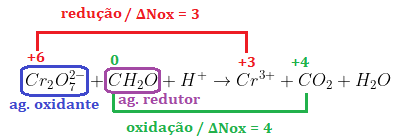
II. É necessário 0,5 L de solução aquosa de dicromato de concentração 0,20 mol·L-1 para oxidar completamente, em meio ácido, 4,50 g de matéria orgânica presente no solo.
Correta. A proporção estequiométrica entre dicromato (Cr2O7-2) e matéria orgânica (CH2O) é 2 mol de Cr2O7-2 : 3 mol de CH2O. Então é preciso calcular a quantidade de dicromato para reagir com 4,50g de CH2O. Para isso, vamos converter a massa de matéria orgânica para quantidade de matéria:
1 mol de CH2O --------- 30 g
x mol de CH2O ---------- 4,50g
x = 0,15 mol de CH2O
Como a proporção é 2 mol de Cr2O7-2 : 3 mol de CH2O, a quantidade de matéria de dicromato necessária para reagir com 0,15 mol de CH2O:
2 mol de Cr2O7-2 ----------- 3 mol de CH2O
y mol de Cr2O7-2 ----------- 0,15 mol de CH2O
y = 0,1 mol de Cr2O7-2
Por fim, calculamos a quantidade de matéria presente em 0,50 L de uma solução 0,20 mol·L-1 de dicromato:
0,20 mol de Cr2O7-2 ------- 1 L
z mol de Cr2O7-2 ----------- 0,50 L
z = 0,1 mol de Cr2O7-2
Então a quantidade de matéria de dicromato presente em 0,5 L de uma solução 0,2 mol/L é igual à quantidade necessária para reagir com 4,50 g de matéria orgânica.
III. Na reação para cada mol de dicromato (Cr2O7-2) que reage são consumidos 8 mol de cátions H+.
Correta. A proporção estequiométrica entre Cr2O7-2 e H+ é 2 mol de Cr2O7-2 : 16 mol de H+. Então, na reação de 1 mol de Cr2O7-2 serão consumidos:
2 mol de Cr2O7-2 -------- 16 mol de H+
1 mol de Cr2O7-2 -------- x mol de H+
x = 8 mol de H+
Então, para cada mol de Cr2O7-2 são consumidos 8 mol de H+.
Como todas estão corretas, o gabarito é letra E.