Questão 10568
PUC 2013
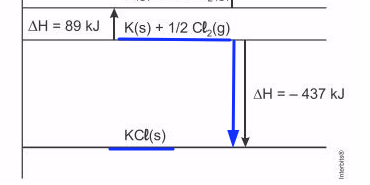
(Pucsp 2013) O estudo da energia reticular de um retículo cristalino iônico envolve a análise do ciclo de Born-Haber. O diagrama de entalpia a seguir exemplifica o ciclo de BornHaber do cloreto de potássio (KCl).
A partir da análise do diagrama é INCORRETO afirmar que
Gabarito:
a entalpia de formação do KCl(s) é de -717 kJ/mol.
Resolução:
a) Correto. A entalpia de sublimação do potássio é de 89 kJ/mol.
b) Correto. A entalpia de ligação Cl—Cl é de 244 kJ/mol.
c) Incorreto. a entalpia de formação do KCl(s) é de -717 kJ/mol.
K(s) + 1/2Cl2(g) → KCl(s)
ΔH = – 437 kJ
d) Correto. o potencial de ionização do K(g) é de 418 kJ mol.
e) Correto. a reação entre o metal potássio e o gás cloro é exotérmica.