Questão 65094
MACKENZIE 2016
(MACKENZIE 2016)
Em 1920, o cientista dinamarquês Johannes N. Brönsted e o inglês Thomas M. Lowry propuseram, independentemente, uma nova definição de ácido e base diferente do conceito até então utilizado de Arrhenius. Segundo esses cientistas, ácido é uma espécie química (molécula ou íon) capaz de doar próton (H+) em uma reação. Já, a base é uma espécie química (molécula ou íon) capaz de receber próton (H+) em uma reação. Abaixo está representada uma reação com a presença de ácidos e bases de acordo com a teoria ácido-base de Brönsted-Lowry.
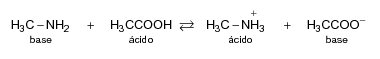
De acordo com essas informações, assinale a alternativa que possui, respectivamente, um ácido e uma base de Brönsted-Lowry.
OH– e NaOH
H3O+ e Cl–
OH– e NH4+
HCN e H3O+
NH3 e H2SO4
Gabarito:
H3O+ e Cl–
Resolução:
A teoria ácido-base de Brönsted-Lowry caracteriza uma substância ácida como a substância capaz de doar um próton e uma substância basica como a que pode receber um próton, analisando as alternativas.
a) OH– e NaOH, incorreta, o OH- não é capaz de doar um próton.
b) H3O+ e Cl–, correta, o íon H3O+ é capaz de doar um próton e formar água, e o íon Cl- é capaz de receber um próton para formar HCl
c) OH– e NH4+, incorreta, nem o íon hidroxila é capaz de doar um próton e nem o íon amônio é capaz de receber um próton.
d) HCN e H3O+, incorreta, o ácido cianídrico é capaz de doar um próton, mas o íon hidrônio é incapaz de receber um próton.
e) NH3 e H2SO4, incorreta.