Questão 62
ITA 2022
(ITA - 2022 - 1ª FASE)
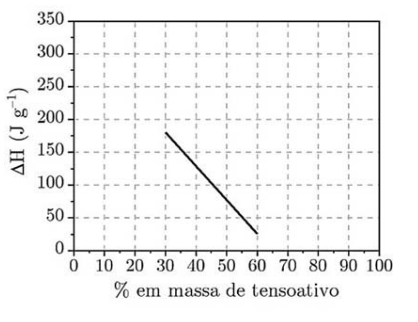
Sistemas compostos por água e tensoativos em diferentes proporções, depois de homogeneizados, passam por um processo termodinâmico quando atingem temperaturas em torno de 0 °C. A variação de entalpia () desse processo foi determinada para cada mistura em função da composição do sistema, conforme apresentado no gráfico. Considere que o ponto de fusão do tensoativo puro é menor que -20 °C e o calor latente de fusão da água pura é de 334 J • g-1. Sobre esses sistemas são feitas as seguintes afirmações:
I. O ΔH refere-se à transição de fase do tensoativo.
II. O calor latente de fusão do tensoativo puro é de -180 J • g-1.
III. Até 35% em massa de água pode ser apresentar na forma associada à substância e não funde.
IV. O ΔH é proporcional à quantidade de água não associada ao tensoativo.
Com base no gráfico e nas informações do enunciado, assinale a opção que indica a(s) afirmação(ões) CORRETA(S).
Apenas I e II
Apenas I, II e IV
Apenas II
Apenas III e IV
Todas
Gabarito:
Apenas III e IV
Resolução:
I. Incorreta. Refere-se ao processo de transformação de fase da água.
II. Incorreta.
Quando x = 0, a porcentagem em massa de água é 100%. Pela extrapolação para x = 0 pode-se determinar o calor latente de fusão da água, que é de 334 J.g-1.
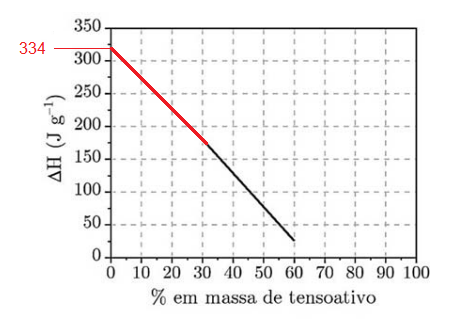
Alternativamente, pode-se pensar que no processo de fusão ocorre absorção de energia, e, portanto o calor latente de fusão não pode ser negativo, o que torna a afirmativa incorreta.
III. Correta.
Quando a massa de água corresponde a 35%, a massa de tensoativo corresponde a 65%. Por extrapolação da reta
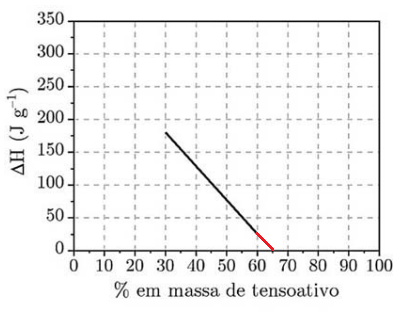
Quando a porcentagem em massa de tensoativo é igual a 65%, ΔH = 0. O processo de fusão é endotérmico e tem ΔH positivo. Portanto, até 35% de massa de água não ocorre a fusão.
IV. Correta.
, em que x é a porcentagem em massa de tensoativo. Se xa é a porcentagem em massa de água, temos
Como a < 0, o ΔH é proporcional à quantidade de água não associada ao tensoativo.