Questão 13
ITA 2017
(ITA - 2017 - 1ª FASE)
A pressão de vapor da água pura é de 23,8 torr a 25 ºC. São dissolvidos 10,0 g de cloreto de sódio em 100,0 g de água pura a 25 ºC. Assinale a opção que indica o valor do abaixamento da pressão de vapor da solução, em torr.
Dados: Massa molar (g/mol): Na = 22,99 ; Cl = 35,45 ; H = 1,01 ; O = 16,00
22,4
11,2
5,6
2,8
1,4
Gabarito:
1,4
Resolução:
Segundo a Lei de Raoult: a pressão máxima de vapor de uma solução diluída (p) de soluto não volátil e não iônico é igual ao produta da pressão máxima de vapor do solvente puro (po) pela fração molar do solvente (x2). Em caso de solutos iônicos, multiplica-se o resultado pelo fator de Van't Hoff (i).
(equação 1)
Como o abaixamento da pressão de vapor pode ser definido como:
(equação 2)
Substituindo a equação 1 na 2:
(equação 3)
Como a soma das frações molares de uma mistura é igual a 1, e nessa questão, só estão presentes dois componentes (água e NaCl):
Logo:
(equação 4)
Substituindo a equação 4 na 3:
(equação 5)
Como foi adicionado um soluto não volátil, é preciso adicionar na fórmula o fator de Van't Hoff (i):
(equação 6)
Numa solução muito diluída, o número de mols do solvente (n2) é muito maior do que o número de mols do soluto (n1). Então,
(equação 7)
Substituindo a equação 7 na equação 6:
(equação 8)
Para fazer os cálculos, é preciso calcular a massa molar do NaCl e do H2O:
NaCl = 58,44g
H2O = 18,02g
Do enunciado, tira-se os valores de massa e também a pressão:
m1 = 10g e m2=100g
po = 23,8torr
O Fator de Van't Hoff é igual ao número de partículas após a dissociação. No caso da água, o fator vai ser igual a 2 já que cada mol de NaCl dissocia em 1 mol de Na+ e 1 mol de Cl-, como pode ser observado abaixo:
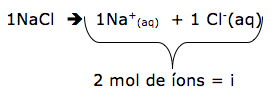
O cálculo detalhado do fator é:
Substituindo as informações calculadas e informadas na equação 8: