Questão 1
ITA 2008
(ITA - 2008 - 2 FASE) Considere as seguintes moléculas no estado gasoso: OF2, BeF2, AlCl2 e AlS2.
a) Dê as estruturas de Lewis e as geometrias moleculares de cada uma das moléculas.
b) Indique as moléculas que devem apresentar caráter polar.
Gabarito:
Resolução:
a) Dê as estruturas de Lewis e as geometrias moleculares de cada uma das moléculas.
► OF2:

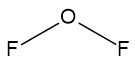
Geometria Angular
► BeF2:
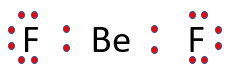
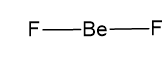
Geometria Linear
► AlCl2:

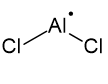
Geometria Angular
► AlS2:

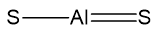
Geometria Linear
b) Indique as moléculas que devem apresentar caráter polar.
Caráter polar são as substâncias que vão apresentar momento dipolo diferente de 0. Quem apresenta geometria linear com os ligantes do átomo central igual terá momento dipolo igual a 0 (AlS2 e BeF2), enquanto que as moléculas angulares terão momento dipolo diferente de 0 (OF2 e AlCl2)