Questão 23
ITA 2007
(ITA - 2007)
Um dos métodos de síntese do clorato de potássio (KClO3) é submeter uma solução de cloreto de potássio (KCl) a um processo eletrolítico, utilizando eletrodos de platina. São mostradas abaixo as semi-equações que representam as semi-reações em cada um dos eletrodos e os respectivos potenciais elétricos na escala do eletrodo de hidrogênio nas condições-padrão (E°):
ELETRODO I: Cl-(aq) + 3 H2O(l) ClO3-(aq) + 6 H+(aq) + 6e- (CM) Eº = 1,45 V
ELETRODO II: 2 OH-(aq) + H2(g) 2 H2O(l) + 2e- (CM) Eº = -0,83 V
(a) Faça um esquema da célula eletrolítica.
(b) Indique o cátodo.
(c) Indique a polaridade dos eletrodos.
(d) Escreva a equação que representa a reação química global balanceada.
Gabarito:
Resolução:
a)
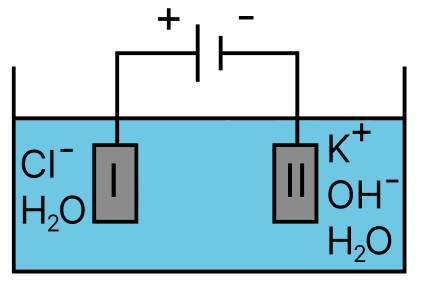
b)
O cátodo é o eletrodo em que ocorre a reação de redução e o ânodo é o eletrodo em que ocorre a reação de oxidação.
A reação representada no eletrodo I é uma reação de oxidação, em que o Cl- é oxidado a ClO3-. Como o objetivo do processo é a formação do KClO3, a reação que ocorre no eletrodo I deve ser a reação de oxidação. Portanto, o cátodo, eletrodo em que ocorre a reação de redução, é o eletrodo II.
c)
Na eletrólise o cátodo é o eletrodo negativo e o ânodo é o eletrodo positivo.
d)
Equação de dissociação do KCl:
KCl(s) → K+(aq) + Cl-(aq)
Equação da reação de redução:
2 H2O(l) + 2e- → 2 OH-(aq) + H2(g)
Equação da reação de oxidação:
Cl-(aq) + 3 H2O(l) → ClO3-(aq) + 6 H+ + 6e-
Para obter a equação global, multiplica-se a equação da reação de redução por 3 e faz-se a soma das três equações:
KCl(s) + 3 H2O(l) → K+(aq) + ClO3-(aq)