Questão 4
ITA 2007
(ITA - 2007)
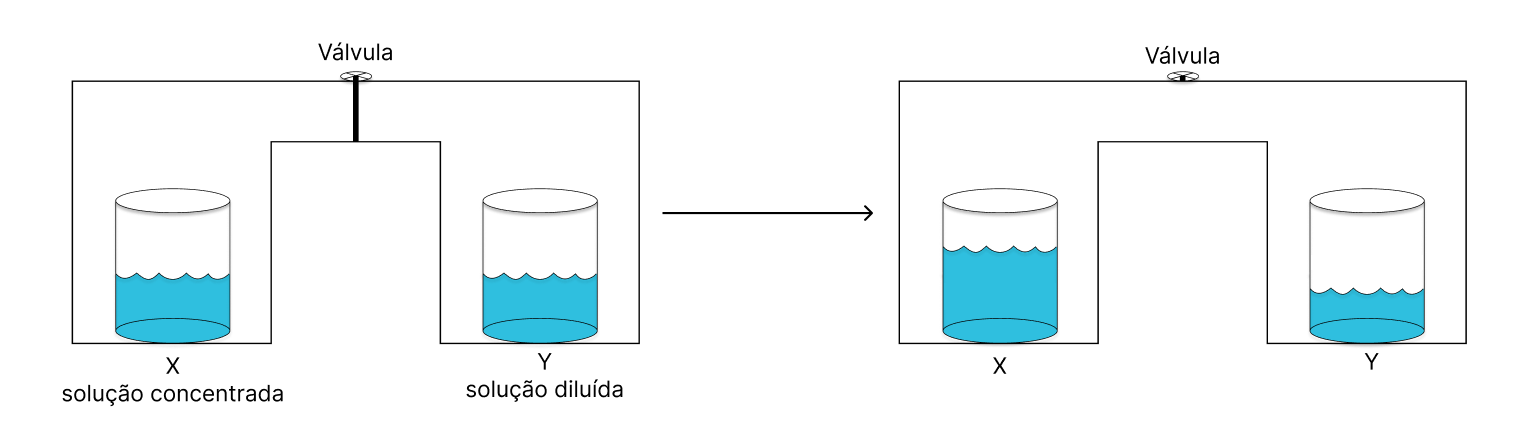
Dois béqueres, X e Y, contêm, respectivamente, volumes iguais de soluções aquosas: concentrada e diluída de cloreto de sódio na mesma temperatura. Dois recipientes hermeticamente fechados, mantidos à mesma temperatura constante, são interconectados por uma válvula, inicialmente fechada, cada qual contendo um dos béqueres. Aberta a válvula, após o restabelecimento do equilíbrio químico, verifica-se que a pressão de vapor nos dois recipientes é Pf.
Assinale a opção que indica, respectivamente, as comparações CORRETAS entre os volumes inicial (VXi) e final (VXf), da solução no béquer X e entre as pressões de vapor inicial (PYi) e final (Pf) no recipiente que contém o béquer Y.
VXi < VXf e PYi = Pf
VXi < VXf e PYi > Pf
VXi < VXf e PYi < Pf
VXi > VXf e PYi > Pf
VXi > VXf e PYi < Pf
Gabarito:
VXi < VXf e PYi > Pf
Resolução:
Como a solução Y é hipotônica em relação a solução X, quando a válvula for aberta ocorrerá migração do solvente da solução Y para X. Após o reestabelecimento do equilíbrio, as concentração das duas soluções são iguais. Portanto, o volume final de X é maior que o volume inicial de X
VXf > VXi ou VXi < VXf
Como ocorre diminuição na quantidade de solvente na solução Y e a quantidade de soluto se mantém a mesma, a concentração da solução Y aumenta. Quanto maior é a concentração de uma solução, menor é sua pressão de vapor. Portanto, a pressão de vapor da solução Y diminui
Pf < PYi ou PYi > Pf