Questão 9
ITA 2007
(ITA - 2007 - 1a Fase)
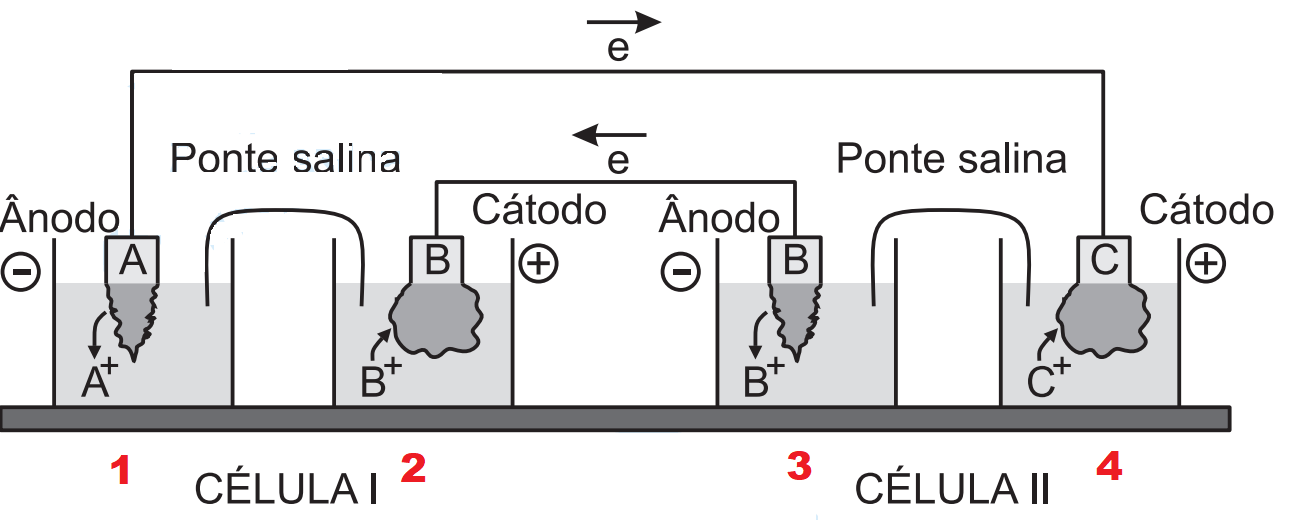
Duas células (I e II) são montadas como mostrado na figura. A célula I consiste de uma placa A(c) mergulhada em uma solução aquosa 1 mol L-1 em AX, que está interconectada por uma ponte salina a uma solução 1 mol L-1 em BX, na qual foi mergulhada a placa B(c). A célula II consiste de uma placa B(c) mergulhada em uma solução aquosa 1 mol L-1 em BX, que está interconectada por uma ponte salina à solução 1 mol L-1 em CX, na qual foi mergulhada a placa C(c). Considere que durante certo período as duas células são interconectadas por fios metálicos, de resistência elétrica desprezível. Assinale a opção que apresenta a afirmação ERRADA a respeito de fenômenos que ocorrerão no sistema descrito.
Dados eventualmente necessários:
E0 A+(aq)/A(c) = 0,400 V;
E0 B+(aq)/B(c) = - 0,700 V e
E0 C+(aq)/C(c) = 0,800 V.
A massa da placa C aumentará.
A polaridade da semicélula B/B+(aq) da célula II será negativa.
A massa da placa A diminuirá.
A concentração de B+(aq) na célula I diminuirá.
A semicélula A/A+(aq) será o cátodo.
Gabarito:
A semicélula A/A+(aq) será o cátodo.
Resolução:
Célula I: Placa A: ânodo (pólo negativo) – massa diminuirá
Placa B: cátodo (pólo positivo) – massa aumentará
Célula II: Placa B: ânodo (pólo negativo) – massa diminuirá
Placa C: cátodo (pólo positivo) – massa aumentará
Cálculo da tensão elétrica para justificar o sentido dos elétrons:
∆Vcélula I = Eºoxi A + Eºred B = -0,400 + (-0,700) = -1,100V
∆Vcélula II = Eºoxi B + Eºred C = 0,700 + (0,800) = +1,500V
Como a célula II apresenta maior ∆V, o sentido dos elétrons será do ânodo da célula II para o cátodo da célula I.