Questão 27
ITA 2001
(ITA - 2001)
Existem três estruturas possíveis para a molécula de PF3(CH3)2, onde o átomo de fósforo é o átomo central. Desenhe as três estruturas e explique como valores de momento de dipolo obtidos experimentalmente podem ser utilizados para distingui-las.
Dados:
números atômicos: H = 1 ; C = 6 ; F = 9 ; P = 15
Gabarito:
Resolução:
A diferença de eletronegatividade entre o flúor e o fósforo é muito maior, por tanto será a definidora da polaridade da molécula. As moléculas têm a forma de uma bipirâmide trigonal.
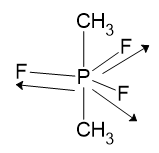
Momento dipolar 1 nulo.
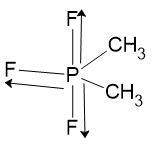
Momento dipolar 2 não nulo ()
Estrutura 1:
Três vetores planos que se anulam e entre eles ângulo de 120°.
Estrutura 2:
O vetor resultante é o momento de uma ligação F-P. Visto que duas delas se anulam.
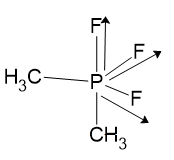
Estrutura 3:
Como o ângulo entre duas das ligações P-F(r) é obtuso o valor resultante é menor que das outras duas ligações P-F(o).
Como o ângulo entre duas das ligações P-F é 90°, o ângulo reto, a resultante será a hipotenusa do triângulo retângulo.
A soma desses três vetores que tem sentidos que se somam, é maior que em 2.
Em ordem de polaridade temos:
III > II > I
