Questão 12
ITA 2001
(ITA - 2001 - 1a Fase)
Considere as seguintes afirmações:
I. O nível de energia de um átomo, cujo número quântico principal é igual a 4, pode ter, no máximo, 32 elétrons.
II. A configuração eletrônica 1s2 2s2 2p2 x 2p2 y representa um estado excitado do átomo de oxigênio.
III. O estado fundamental do átomo de fósforo contém três elétrons desemparelhados.
IV. O átomo de nitrogênio apresenta o primeiro potencial de ionização menor que o átomo de flúor.
V. A energia necessária para excitar um elétron do estado fundamental do átomo de hidrogênio para o orbital 3s é igual àquela necessária para excitar este mesmo elétron para o orbital 3d.
Dado P (Z = 15); O (Z = 8)
Das afirmações feitas, estão CORRETAS
apenas I, II e III.
apenas I, II e V.
apenas III e IV.
apenas III, IV e V.
todas.
Gabarito:
todas.
Resolução:
- n: número quântico principal (camada)
- l: número quântico secundário ou azimutal (subnível)
- ml: número quântico magnético (orientação dos orbitais)
- ms: spin (sentido da rotação do elétron)
I. Quando n = 4, teremos os subníveis: s, p, d e f. Cada uma recebe, no máximo, 2, 6, 10 e 14 elétrons, respectivamente.
CORRETA. 2 + 6 + 10 + 14 = 32 elétrons no máximo.
II. A configuração eletrônica 1s2 2s2 2p2 x 2p2 y representa um estado excitado do átomo de oxigênio.
CORRETA. No estado fundamental, o átomo de oxigênio apresenta subnível p:
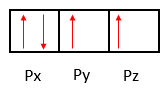
No estado excitado, temos:
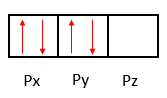
III. O estado fundamental do átomo de fósforo contém três elétrons desemparelhados.
CORRETO. A configuração eletrônica do fósforo é: 1s2 2s2 2p6 3s2 3p3 . Dessa forma, ele vai apresentar 3 elétrons no último subnível e estão desemparelhados.
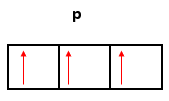
IV. O átomo de nitrogênio apresenta o primeiro potencial de ionização menor que o átomo de flúor.
CORRETO. O potencial de ionização do flúor é 17,42, enquanto que o do nitrogênio é de 14,53.
V. A energia necessária para excitar um elétron do estado fundamental do átomo de hidrogênio para o orbital 3s é igual àquela necessária para excitar este mesmo elétron para o orbital 3d.
CORRETO. A energia é a mesma para levar um elétron do nível 1 para o nível 3 do hidrogênio.