Questão 9
IME 2021
(IME - 2021/2022 - 2ª fase)
Na figura abaixo, apresenta-se um conjunto cilindro-pistão, onde o peso do pistão é desprezível, em que ocorre a seguinte reação do óxido de níquel (II) à temperatura constante:
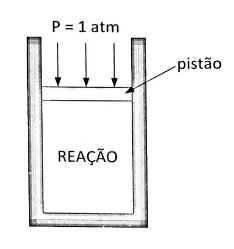
Para a manutenção da temperatura constante até a situação de equilíbrio, devem ser retirados do meio reacional 16,10 kJ de energia por mol de óxido de níquel reagido, na forma de calor. Sabe-se que a constante de equilíbrio para a reação é e que, na temperatura de reação, as entropias padrão são:
;
;
; e
.
Com base nas informações fornecidas e considerando que os gases se comportam idealmente, determine a temperatura na qual a reação foi conduzida.
Gabarito:
Resolução:
Para a reação ficar em equilíbrio, a variação da energia de Gibbs deve ser igual a 0. Essa variação pode ser calculada por:
Como ainda não foi alcançado o equilíbrio, pode-se relacionar a constante de equilíbrio (K) e a energia de Gibbs pela equação:
Portanto
(equação 1)
Pode-se calcular pelos dados do exercício:
Ocorre liberação de 16,1 kJ/mol de energia. Portanto, o valor do ΔH é
Como R é uma constante e foi dado o valor de K, pode-se calcular a temperatura substituindo os valores na equação 1
Isolando T: