Questão 34
IME 2014
[IME - 2014/2015 - 1a fase]
Considere os compostos abaixo enumerados.
I. Acetona;
II. Neopentano;
III. Flureto de lítio;
IV. Etanamida;
V. Pentano;
Assinale a alternativa que apresenta a sequência correta, conforme a ordem crescente de ponto de ebulição.
III, I, IV, II, V
V, II, I, IV, III.
II, V, I, IV, III.
II, V, IV, I, III.
V, II, III, IV, I.
Gabarito:
II, V, I, IV, III.
Resolução:
Analisando cada composto:
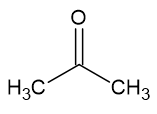
I. Acetona;
A interação entre as moléculas da acetona é por dipolo permanente.
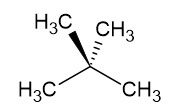
II. Neopentano;
Hidrocarboneto, com cadeia ramificada, em que suas moléculas vão interagir por forças de Van der Waals.
III. Flureto de lítio;
O fluoreto de lítio é um composto iônico.
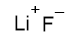
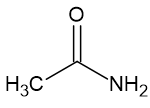
IV. Etanamida;
As moléculas desse composto vão interagir, principalmente, por ligações ou ponte de hidrogênio.
V. Pentano;
Hidrocarboneto, com cadeia simples, em que suas moléculas vão interagir por forças de Van der Waals.
Os compostos iônicos vão apresentar maior força entre as ligações e, por isso, maior ponto de ebulição. Em seguida, compostos que realizam interação por ligação de hidrogênio terão ponto de ebulição mais alto e vindo logo atrás, em ordem, dipolo permanente e dipolo induzido.Entre os hidrocarbonetos, o que apresenta maior ponto de ebulição é o composto que apresenta cadeia simples.
A ordem crescente de ponto de ebulição será: Neopentano > Pentano > Acetona > Etanamida > Fluoreto de Lítio