Questão 7
FUVEST 2016
(FUVEST - 2016 - 2ª Fase)
A hortênsia (Hydrangea macrophylla) produz flores azuis quando cultivada em solo de pH < 5. Quando o pH do solo é maior do que 5, as flores tornamse rosadas. Um jardineiro recebeu uma encomenda de hortênsias rosadas. Ele dispõe de um jardim plano, com as formas e dimensões descritas na figura abaixo, e cujo solo apresenta pH = 4. Para obter um solo adequado à produção de flores rosadas, o jardineiro deverá adicionar uniformemente 300 g de calcário dolomítico por m2 de terreno.

a) Calcule a massa, em quilogramas, de calcário dolomítico necessária para a correção do solo do jardim.
O calcário dolomítico é uma mistura de carbonato de cálcio e carbonato de magnésio. Ao adquirir um pacote desse produto, o jardineiro observou que, no rótulo, sua composição estava expressa na forma das porcentagens, em massa, dos óxidos de cálcio e de magnésio que poderiam ser obtidos a partir dos correspondentes carbonatos contidos no calcário dolomítico.
b) Calcule a porcentagem, em massa, de carbonato de magnésio presente no calcário dolomítico adquirido pelo jardineiro.
Gabarito:
Resolução:
a) Calcule a massa, em quilogramas, de calcário dolomítico necessária para a correção do solo do jardim.
3Kg
O primeiro passo é calcular a área do jardim:
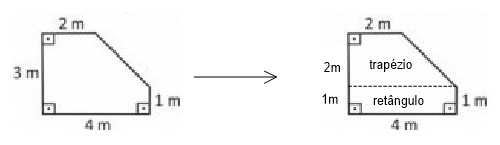
Sabemos que o jardineiro deverá adicionar uniformemente 300 g de calcário dolomítico por m2 de terreno, sendo assim:
b) Calcule a porcentagem, em massa, de carbonato de magnésio presente no calcário dolomítico adquirido pelo jardineiro.
42%
No calcário tem 20% de MgO, vamos usar 100g como parâmetro para calcular a quantidade de MgO em 3kg de calcário:
Como os óxidos de cálcio e de magnésio que poderiam ser obtidos a partir dos correspondentes carbonatos contidos no calcário dolomítico. Temos a reação:
A massa molar de MgCO3 é 84g, e do MgO é 40g. A estequiometria da reação é de 1:1, dessa forma:
Por último, calculamos a porcentagem referente a esse valor: