Questão 78
FUVEST 2006
(FUVEST - 2006 - 1 FASE )
Em determinado processo industrial, ocorre uma transformação química, que pode ser representada pela equação genérica
x A(g) + y B(g) ⇌ z C(g)
em que x, y e z são, respectivamente, os coeficientes estequiométricos das substâncias A, B e C.
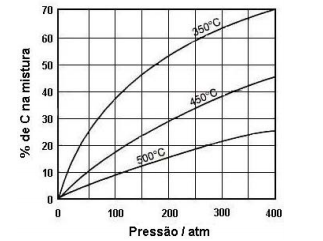
O gráfico representa a porcentagem, em mols, de C na mistura, sob várias condições de pressão e temperatura. Com base nesses dados, pode-se afirmar que essa reação é
a) exotérmica, sendo x + y = z
endotérmica, sendo x + y < z
exotérmica, sendo x + y > z
endotérmica, sendo x + y = z
endotérmica, sendo x + y > z
Gabarito:
exotérmica, sendo x + y > z
Resolução:
O aumento da temperatura favorece reações endotérmicas e a diminuição da temperatura favorece reações exotérmicas. A porcentagem de C na mistura aumenta com a diminuição da temperatura, então a reação é exotérmica no sentido direto.
O aumento da pressão favorece a reação no sentido de produção da menor quantidade de gases. A diminuição da pressão favorece a reação no sentido de produção da maior quantidade de gases. No gráfico da questão a pressão aumenta da esquerda para a direita. Para uma mesma temperatura, a porcentagem de C aumenta com o aumento da pressão, então z é menor que x + y.
Portanto, a alternativa correta é a letra c) exotérmica, sendo x + y > z.