Questão 70
FUVEST 2006
(FUVEST - 2006 - 1 FASE )
A efervescência observada, ao se abrir uma garrafa de champanhe, deve-se à rápida liberação, na forma de bolhas, do gás carbônico dissolvido no líquido. Nesse líquido, a concentração de gás carbônico é proporcional à pressão parcial desse gás, aprisionado entre o líquido e a rolha. Para um champanhe de determinada marca, a constante de proporcionalidade (k) varia com a temperatura, conforme mostrado no gráfico.
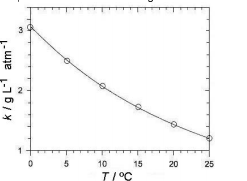
Uma garrafa desse champanhe, resfriada a 12 ºC, foi aberta à pressão ambiente e 0,10 L de seu conteúdo foram despejados em um copo. Nessa temperatura, 20% do gás dissolvido escapou sob a forma de bolhas. O número de bolhas liberadas, no copo, será da ordem de

102
104
105
106
108
Gabarito:
106
Resolução:
Essa é a equação de Lei de Henry:
, em que:
• K é a constante de Henry (g.L-1atm-1)
• P é a pressão (atm)
• C é a concentração (g.L-1)
Para calcular a massa de CO2 dissolvida na garrafa, podemos reescrever a concentração como C=m/V:
Os valores de P e V são conhecidos:
P = 6atm
V = 0,10L
O valor de K é obtido a partir da análise do gráfico. O valor de K para a temperatura de 12ºC é próximo de 1,8g.L-1atm-1.
K = 1,8g.L-1atm-1
Substituição de K, P e V na equação da massa:
O volume de CO2 correspondente a essa massa pode ser calculado a partir do volume molar, dado fornecido na tabela da questão. O volume molar a 12ºC é 24L.mol-1. Isto é, 1mol de gás ocupa 24L. A massa molar do CO2 é 44g.mol-1, então 44g de CO2 ocupam um volume de 24L.
Volume ocupado por 1,08g de CO2:
1 mol CO2 _______ 24 L
44g CO2 ________ 24 L
1,08g CO2 ______ VCO2
Como 20% desse volume escapou na forma de bolhas:
O número de bolhas é o volume de CO2 que escapou dividido pelo volume de cada bolha:
A ordem de grandeza desse valor é 106.