Questão 44846
FUVEST 2006
(FUVEST - 2006)
Em solução aquosa, iodeto de potássio reage com persulfato de potássio (K2S2O8 ).
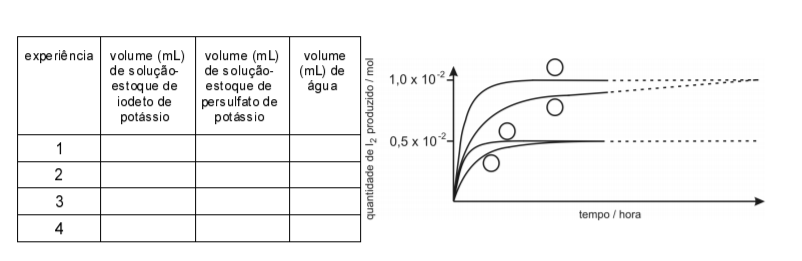
Há formação de iodo e de sulfato de potássio. No estudo cinético desta reação, foram realizadas quatro experiências. Em cada uma delas, foram misturados volumes adequados de soluções-estoque dos dois reagentes, ambas de concentração 4,0 × 10-1 mol / L e, a seguir, foi adicionada água, até que o volume final da solução fosse igual a 1,00 L.
Na tabela, estão indicadas as concentrações iniciais dos reagentes, logo após a mistura e adição de água (tempo igual a zero).
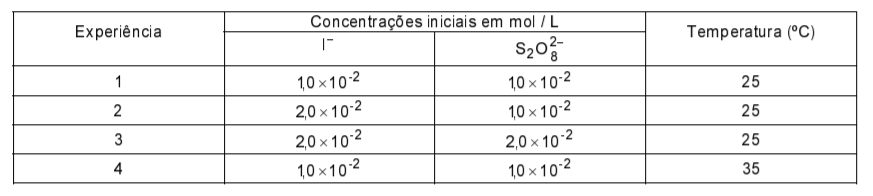
Na página ao lado, está o gráfico correspondente ao estudo cinético citado e, também, uma tabela a ser preenchida com os volumes das soluções-estoque e os de água, necessários para preparar as soluções das experiências de 1 a 4.
a) Escreva a equação química balanceada que representa a reação de oxirredução citada.
b) Preencha a tabela da página ao lado
. c) No gráfico, preencha cada um dos círculos com o número correspondente à experiência realizada. Justifique sua escolha com base em argumentos cinéticos e na quantidade de iodo formado em cada experiência.
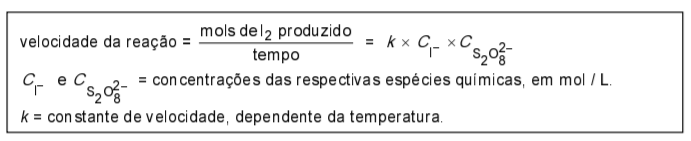
Tabela e gráfico:
Gabarito:
Resolução:
a) 2KI + 1K2S2O8 → 2K2SO4 + I2
b) Cálculo do volume de solução 4,0 . 10 –1 mol/L de KI ou de K2S2O8 necessário para preparar 1L de solução 1,0 . 10 –2 mol/L de KI ou de K2S2O8 :
1L ––––– 4,0 . 10 –1 mol
x ––––– 1,0 . 10 – 2 mol
x = 25 mL
Cálculo do volume de solução 4,0 . 10 –1 mol/L de KI ou de K2S2O8 necessário para preparar 1L de solução 2,0 . 10 –2 mol/L de KI ou K 2S2O8 :
1L ––––– 4,0 . 10 –1 mol
y ––––– 2,0 . 10 –2 mol
y = 50 mL
Volume de água em cada experiência:
Exp 1 = 1000 mL – (25 mL + 25 mL) = 950 mL
Exp 2 = 1000 mL – (50 mL + 25 mL) = 925 mL
Exp 3 = 1000 mL – (50 mL + 50 mL) = 900 mL
Exp 4 = 1000 mL – (25 mL + 25 mL) = 950 mL