Questão 72
FUVEST 2002
(FUVEST - 2002 - 1a fase)
Considere três metais A, B e C, dos quais apenas A reage com ácido clorídrico diluído, liberando hidrogênio. Varetas de A, B e C foram espetadas em uma laranja, cujo suco é uma solução aquosa de pH = 4. A e B foram ligados externamente por um resistor (formação da pilha 1). Após alguns instantes, removeu-se o resistor, que foi então utilizado para ligar A e C (formação da pilha 2).
Nesse experimento, o pólo positivo e o metal corroído na pilha 1 e o pólo positivo e o metal corroído na pilha 2 são, respectivamente,
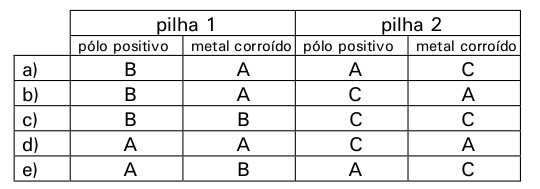
letra a.
letra b.
letra c.
letra d.
letra e.
Gabarito:
letra b.
Resolução:
A transformação de HCl em H2 é uma reação de redução do hidrogênio, já que o nox varia de +1 para 0. Se na presença do metal A o hidrogênio reduz, isso implica que o potencial de redução de A é menor que o hidrogênio. Como o enunciado informa que apenas A reage com HCl formando H2, os demais metais (B e C) possuem potencial de redução maior que o do hidrogênio, que permanece na forma oxidada.
Portanto, se o potencial de redução de A é menor que do hidrogênio também será menor que o de B e C.
Ao ligar os metais A e B em uma solução ácida, o metal B irá reduzir então se encontrará no polo positivo (catodo). E o metal A irá sofrer a corrosão, no polo negativo (ânodo).
Já ao ligar os metais A e C, o metal C irá reduzir no cátodo (+) e A será corroído no ânodo (-).
Gabarito: letra B