Questão 4026
FUVEST 1991
Enche-se uma seringa com pequena quantidade de água destilada a uma temperatura um pouco abaixo da temperatura de ebulição. Fechando o bico, como mostra a figura A a seguir, e puxando rapidamente o êmbolo, verifica-se que a água entra em ebulição durante alguns instantes (veja figura B). Podemos explicar este fenômeno considerando que:
na água há sempre ar dissolvido e a ebulição nada mais é do que a transformação do ar dissolvido em vapor.
com a diminuição da pressão a temperatura de ebulição da água fica menor do que a temperatura da água na seringa.
com a diminuição da pressão há um aumento da temperatura da água na seringa.
o trabalho realizado com o movimento rápido do êmbolo se transforma em calor que faz a água ferver.
calor específico da água diminui com a diminuição da pressão.
Gabarito:
com a diminuição da pressão a temperatura de ebulição da água fica menor do que a temperatura da água na seringa.
Resolução:
O diagrama de estados da água é esboçado assim:
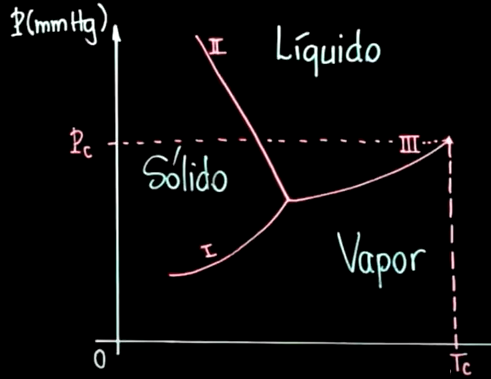
Portanto, ao diminuirmos a pressão muito rapidamente(não dando tempo para que a temperatura do líquido varie tanto), iremos acabar cruzando a linha que separa os estados líquido e vapor do diagrama acima. Essa linha representa justamente os pares de temperatura e pressão em que observa-se o fenômeno da ebulição.
Ou seja, observaremos a ebulição acontecer justamente porque a temperatura de ebulição para aquela nova pressão é menor que a temperatura do líquido, como indica a alternativa B.