Questão 2
ESPCEX 2017
(EsPCEx - 2017)
A emissão de gases derivados do enxofre, como o dióxido de enxofre (SO2), pode ocasionar uma série de problemas ambientais e a destruição de materiais como rochas e monumentos à base de calcita (carbonato de cálcio). Essa destruição ocasiona reações com a emissão de outros gases, como o gás carbônico (CO2), potencializando o efeito poluente. Considerando as equações das reações sucessivas a 27 ºC e 1 atm, admitindo-se os gases como ideais e as reações completas, o volume de CO2 produzido a partir da utilização de 2 toneladas de SO2 como reagente é, aproximadamente:
Dados:
- Massas Atômicas: S = 32 u; O = 16 u; H = 1 u; C = 12 u; Ca = 40 u
- Constante dos gases ideais: R = 0,082 atm . L . mol -1 . K -1
- Volume molar nas condições em que ocorreu a reação (27º e 1 atm) = 24,6 L/mol
4,35 . 106 L de CO2
2,25 . 106 L de CO2
4,75 . 104 L de CO2
5,09 . 103 L de CO2
7,69 . 105 L de CO2
Gabarito:
7,69 . 105 L de CO2
Resolução:
As equações apresentadas ocorrem sucessivamente, então, a equação global é obtida com a soma das etapas:
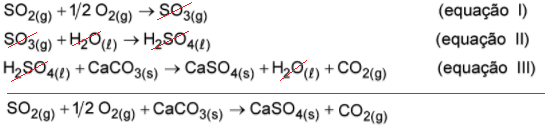
A proporção em quantidade de matéria de SO2 e CO2 é 1:1. Como a questão pede o volume de CO2, é possível criar uma proporção entre a massa de SO2 e o volume de CO2, sendo necessário calcular a massa molar do SO2:
A proporção é:
1 mol de SO2 ------------ 1 mol de CO2
64 g de SO2 -------------- 24,6 L de CO2
Como a questão pergunta o volume de SO2 obtido a partir de 2 toneladas (2x106 g) de SO2:
64 g de SO2 -------------- 24,6 L de CO2
2x106 g de SO2 --------- x
x = 7,69 x 105 L de CO2
O volume obtido de CO2 é 7,69 x 105 L.