Questão 110
ENEM 2023
(ENEM - 2023)
Um assistente de laboratório precisou descartar sete frascos contendo solução de nitrato de mercúrio(I) que não foram utilizados em uma aula prática. Cada frasco continha 5,25 g de Hg2(NO3)2 dissolvidos em água. Temendo a toxidez do mercúrio e sabendo que o Hg2Cl2 tem solubilidade muito baixa, o assistente optou por retirar o mercúrio da solução por precipitação com cloreto de sódio (NaCl), conforme a equação química:
Na dúvida sobre a massa de NaCl a ser utilizada, o assistente aumentou gradativamente a quantidade adicionada em cada frasco, como apresentado no quadro.
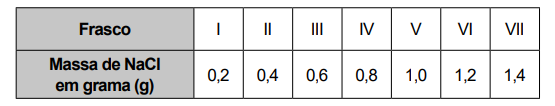
O produto obtido em cada experimento foi filtrado, secado e teve sua massa aferida. O assistente organizou os resultados na forma de um gráfico que correlaciona a massa de NaCl adicionada com a massa de Hg2Cl2 obtida em cada frasco. A massa molar do Hg2(NO3)2 é 525 g mol-1, a do NaCl é 58 g mol-1, e a do Hg2Cl2 é 472 g mol-1.
Qual foi o gráfico obtido pelo assistente de laboratório?
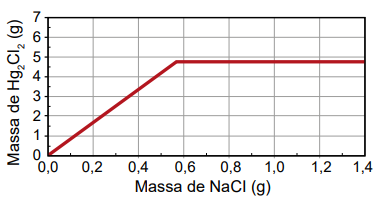
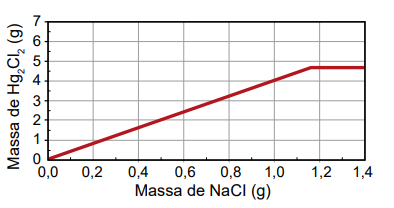
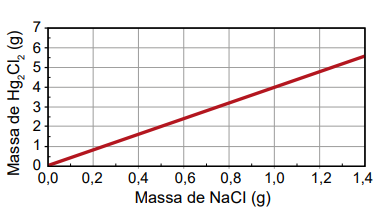
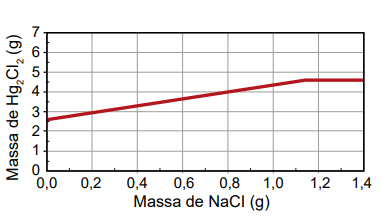
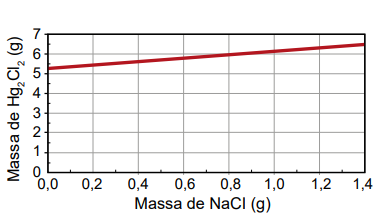
Gabarito:

Resolução:
A reação de formação do cloreto de mercúrio pode ser descrita como:
Se em cada frasco há 5,25g de Hg2(NO3)2, podemos calcular a quantidade de NaCl necessário para converter todo o nitrato de mercúrio em cloreto de mercúrio.
Pela estequiometria:
1 mol de Hg2(NO3)2 ---- 2 mols de NaCl
525 g de Hg2(NO3)2 ---- 2*58 g de NaCl
5,25 g de Hg2(NO3)2 ---- X g de NaCl
Após calcular, podemos concluir que é necessário utilizar 1,16 g de NaCl para reagir com todo o 5,25g de Hg2(NO3)2. Sendo assim, após essa massa de NaCl o gráfico de Hg2Cl2 é constante.
Sendo assim, a alternativa que melhor descreve essa situação é
Alternativa b)
