Questão 111
ENEM 2017
(ENEM/PPL - 2017)
Alguns profissionais burlam a fiscalização quando adicionam quantidades controladas de solução aquosa de hidróxido de sódio a tambores de leite de validade vencida. Assim que o teor de acidez, em termos de ácido láctico, encontra-se na faixa permitida pela legislação, o leite adulterado passa a ser comercializado. A reação entre o hidróxido de sódio e o ácido láctico pode ser representada pela equação química:
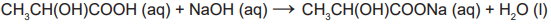
A consequência dessa adulteração é o(a)
aumento do pH do leite.
diluição significativa do leite.
precipitação do lactado de sódio.
diminuição da concentração de sais.
aumento na concentração de íons H+.
Gabarito:
aumento do pH do leite.
Resolução:
a) Correta. O Na(OH) é uma base forte e os ácidos orgânicos são considerados fracos ou médio , dessa forma o sal gerado possui caráter básico. Então mesmo que ocorra a neutralização da base com o ácido gerando sal, o próprio sal gerado possuí caráter básico, aumentando dessa forma o pH.
b) Incorreto: Isso ocorreria caso fosse adicionada água ao leite.
c) Incorreto: Na equação química no enunciado o sal formado encontra-se no estado aquoso (aq).
d) Ocorre um aumento na concentração de sais devido a produção de lactato de sódio.
e) A adição de base diminui a concentração de íons H+