Questão 81
ENEM 2011
(ENEM - 2011)
O peróxido de hidrogênio é comumente utilizado como antisséptico e alvejante. Também pode ser empregado em trabalhos de restauração de quadros enegrecidos e no clareamento de dentes. Na presença de soluções ácidas de oxidantes, como o permanganato de potássio, este óxido decompõe-se, conforme a equação a seguir:
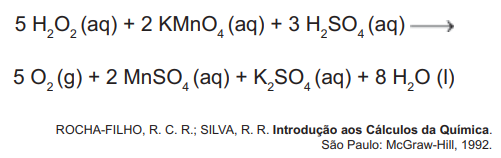
De acordo com a estequiometria da reação descrita, a quantidade de permanganato de potássio necessária para reagir completamente com 20,0 mL de uma solução 0,1 mol/L de peróxido de hidrogênio é igual a:
2,0×100 mol.
2,0×10-3 mol.
8,0×10-1 mol.
8,0×10-4 mol.
Gabarito:
8,0×10-4 mol.
Resolução:
Cálculo da quantidade de matéria em 20mL da solução de H2O2 de concentração 0,1mol.L-1:
A concentração é a razão entre a quantidade de matéria e o volume:
Então podemos calcular a quantidade de matéria pela multiplicação entre concentração e volume:
Analisando a estequiometria da reação a partir da equação:
5 H2O2 (aq) + 2 KMnO4 (aq) + 3 H2SO4 (aq) → 5 O2 (g) + 2 MnSO4 (aq) + K2SO4 (aq) + 8 H2O (l)
Vemos que 5mol de H2O2 reage com 2mol de KMnO4. Podemos montar a seguinte regra de três para calcular a quantidade de matéria de KMnO4 que reage com 0,002mol de H2O2:
5mol H2O2 ______________ 2mol de KMnO4
0,002mol de H2O2 ________ x
Alternativa correta é Letra D.