Questão 18751
UNIFESP 2006
(Unifesp 2006) A geometria molecular e a polaridade das moléculas são conceitos importantes para predizer o tipo de força de interação entre elas. Dentre os compostos moleculares nitrogênio, dióxido de enxofre, amônia, sulfeto de hidrogênio e água, aqueles que apresentam o menor e o maior ponto de ebulição são, respectivamente,
SO2 e H2S.
N2 e H2O.
NH3 e H2O.
N2 e H2S.
SO2 e NH3.
Gabarito:
N2 e H2O.
Resolução:
A temperatura de ebulição está diretamente relacionada com a força das interações intermoleculares, isso significa que quanto maios forte for a interação, maior o ponto de ebulição.
As estruturas das moléculas nitrogênio, dióxido de enxofre, amônia, sulfeto de hidrogênio e água, e as suas interações intermoleculares são:
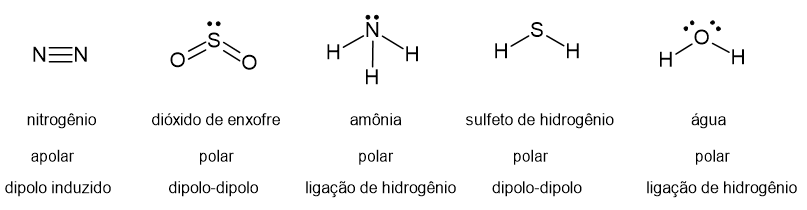
Das interações presentes nessas moléculas, a dipolo induzido é a menos intensa, portanto vai ter o menor ponto de ebulição.
Já a interação mais forte vai ser a ligação de hidrogênio presente na água e na amônia. Como o empacotamento da molécula de água é melhor, o ponto de ebulição também vai maior.
Portanto, o menor ponto de ebulição é do N2 e o maior vai ser o da água.