Questão 19
UNICAMP 2024
(UNICAMP - 2024)
O oxalato de cálcio em humanos está associado a calcificações benignas do tecido mamário e a pedras nos rins. Em indivíduos saudáveis, a urina é tipicamente supersaturada em oxalato de cálcio. O desenvolvimento de pedras nos rins, por outro lado, é prevenido por proteínas e pequenas moléculas contendo grupos carboxilatos.
a) Considerando o que se informa no texto, escreva uma equação química e a expressão da constante de equilíbrio associada, que representam a formação da pedra no rim. O texto informa que a urina é supersaturada em oxalato de cálcio; o que isso significa conceitualmente, isto é, do ponto de vista do equilíbrio químico?
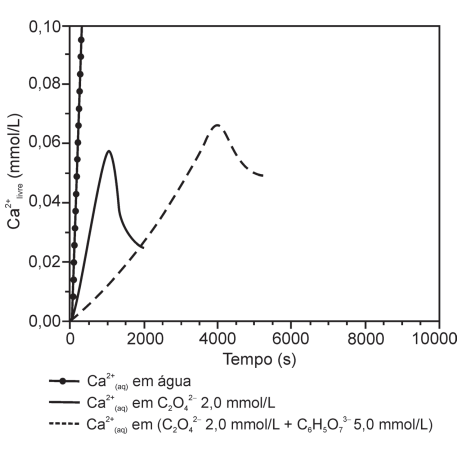
b) Pesquisadores avaliaram como a concentração de cálcio livre (Ca2+) em solução varia quando se adiciona Ca2+(aq) em soluções contendo oxalato de concentração 2 mmol/L e diferentes concentrações de citrato, conforme a figura. Os dados permitem inferir que o citrato pode ser um agente terapêutico na prevenção de pedra no rim. Faça uma descrição quantitativa de modo a justificar, do ponto de vista do equilíbrio químico, a afirmação sobre a função do citrato na prevenção de pedra no rim.
Dados:
Oxalato: C2O42- ; citrato: C6H5O73- .
Gabarito:
Resolução:
a)
A equação de formação é
Sendo assim, quanto maior a concentração do íon oxalato (solução saturada), mais favorecida é a produção do sal oxalato de calcio devido o deslocamento de equilíbrio na direção dos produtos.
b) A linha contínua mostra a concentração do Ca+2 livre em solução em uma solução com íons oxalato, dessa forma, é possível notar que a concentração aumenta até que se atinja o permitido pelo Kps. Já a linha tracejada ilustra a concentração de cálcio livre em uma solução contendo íons citrato e oxalato, é possível notar que a presença do íon citrato permite maior concentração de cálcio livre por mais tempo, isto se deve à complexação dos íons cálcio com o íon citrato, logo, a formação de oxalato de cálcio só ocorre após consumo dos íons citrato.