Questão 49
UNESP 2023
(UNESP - 2023)
Analise os diagramas de entalpias de reações parciais, associadas com a reação de cal viva sólida, CaO (s), com água líquida, para a produção de cal hidratada sólida, Ca(OH)2 (s).
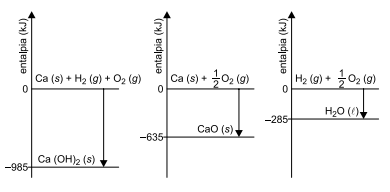
A variação de entalpia dessa reação de cal viva com água líquida, para produzir cal hidratada, é igual a
- 1905 kJ/mol.
- 65 kJ/mol.
+ 95 kJ/mol.
- 1620 kJ/mol.
+ 2890 kJ/mol.
Gabarito:
- 65 kJ/mol.
Resolução:
Pelos gráficos, podemos obter que as entalpias de formação das substâncias são,
Ca(OH)2 : ΔHf = – 985 kJ/mol
CaO : ΔHf = – 635 kJ/mol
H2O : ΔHf = – 285 kJ/mol
A reação citada no enunciado é,
CaO(s) + H2O(l) → Ca(OH)2
Logo, podemos calcular a entalpia da reação a partir das entalpias de formação, seguindo a fórmula abaixo,
, desta forma,