Questão 16
UNESP 2018
(UNESP - 2018 - 2ª FASE)
No cultivo hidropônico, a composição da solução nutritiva deve ser adequada ao tipo de vegetal que se pretende cultivar. Uma solução específica para o cultivo do tomate, por exemplo, apresenta as seguintes concentrações de macronutrientes:
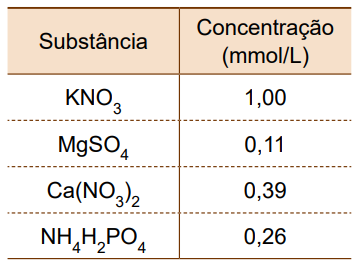
(Maria C. L. Braccini et al. Semina: Ciências agrárias, março de 1999.)
Durante o desenvolvimento das plantas, é necessário um rígido controle da condutividade elétrica da solução nutritiva, cuja queda indica diminuição da concentração de nutrientes. É também necessário o controle do pH dessa solução que, para a maioria dos vegetais, deve estar na faixa de 5,0 a 6,5.
a) Por que a solução nutritiva para o cultivo hidropônico de tomate é condutora de eletricidade? Calcule a quantidade, em mmol, do elemento nitrogênio presente em 1,0 L dessa solução.
b) Considere que 1,0 L de uma solução nutritiva a 25oC, inicialmente com pH = 6,0, tenha, em um controle posterior, apresentado o valor mínimo tolerável de pH = 4,0. Nessa situação, quantas vezes variou a concentração de íons H+(aq)? Sabendo que o produto iônico da água, Kw, a 25oC, é igual a 1,0x10-14, calcule as quantidades, em mol, de íons OH-(aq) presentes, respectivamente, na solução inicial e na solução final.
Gabarito:
Resolução:
a) A soulçao é condutora de eletricidade por que há íons dissolvidos nela.
Os macronutrientes que vão liberar nitrogênio seguem a seguinte proporção estequiométrica:
l.
ll.
lll.
Logo, a quantidade de nitrogênio liberada vai ser a somar esquiométrica liberada pela dissociação de cada um dos macronutrientes em 1 litro será:
b) Sabendo que
e
Logo,
H2 é 100 vezes maior do que H1.