Questão 72
UNESP 2016
(UNESP - 2016 - 1ª FASE) A luz branca é composta por ondas eletromagnéticas de todas as frequências do espectro visível. O espectro de radiação emitido por um elemento, quando submetido a um arco elétrico ou a altas temperaturas, é descontínuo e apresenta uma de suas linhas com maior intensidade, o que fornece “uma impressão digital” desse elemento. Quando essas linhas estão situadas na região da radiação visível, é possível identificar diferentes elementos químicos por meio dos chamados testes de chama. A tabela apresenta as cores características emitidas por alguns elementos no teste de chama:
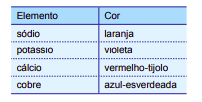
Uma estudante preparou 10,0 mL de uma solução 1,00 mol·L–1 de cloreto de um dos metais apresentados na tabela do texto a fim de realizar um teste de chama em laboratório. No teste de chama houve liberação de luz vermelha intensa. A partir das informações contidas no texto e utilizando a classificação periódica dos elementos, assinale a alternativa que apresenta a massa do sal utilizado pela estudante, em gramas, e a sua fórmula.
1,11 e CaCl2 .
7,56 e CaCl.
11,1 e CaCl2.
0,756 e CaCl.
0,111 e CaCl2 .
Gabarito:
1,11 e CaCl2 .
Resolução:
Como houve liberação de luz VERMELHA, sabemos que o elemento usado foi o Ca (cálcio) segundo a tabela fornecida. O cálcio é da família 2A, portanto apresenta 2 elétrons na sua camada de valência sendo seu cátion representado por : Ca2+
Assim, a fórmula do sal usado é CaCl2
Usando a concentração da solução em mol/L temos:
1mol _______ 1000 ml (1 L)
x (mols)_____ 10 (ml)
Fazendo a regra de três, teremos:
x= 0,01 mol de CaCl2
Usando a massa molar podemos descobria a massa do sal utilizado:
MMCaCl2 = 111 g/mol
1 mol _______ 111 g de CaCl2
0,01mol_____ y (g) de CaCl2
Resolvendo a regra de três, teremos:
y= 1,11 g de CaCl2 utilizada.
Portanto, LETRA A.