Questão 49
UFU 2019
(UFU - 2019 - 1ª FASE ) Os experimentos ilustrados utilizaram, nas três situações, quantidades iguais de massa de carbonato de cálcio e mesma concentração e volumes de ácido sulfúrico. Na seringa, foi coletado o gás carbônico como um dos produtos dessa reação. A partir desses experimentos, deduz-se que, após reação total nos três casos,
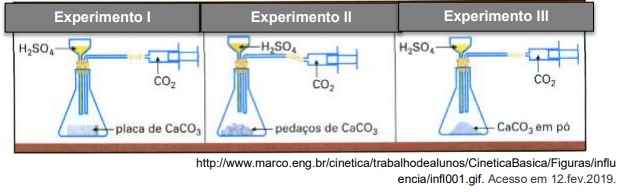
o tempo necessário para se produzir a mesma quantidade de gás carbônico foi maior no experimento I, pois na placa a superfície de contato é menor.
a quantidade de gás carbônico produzida no experimento II é menor que aquela produzida no experimento III, pois o carbonato estava despedaçado.
o volume de gás carbônico verificado na seringa no experimento III é menor que o volume do mesmo gás na seringa do experimento I, em função da pulverização do carbonato.
o efeito do ácido sulfúrico na reação do experimento I é diferente do efeito no experimento II, produzindo uma mistura de gases, além do gás carbônico.
Gabarito:
o tempo necessário para se produzir a mesma quantidade de gás carbônico foi maior no experimento I, pois na placa a superfície de contato é menor.
Resolução:
a) o tempo necessário para se produzir a mesma quantidade de gás carbônico foi maior no experimento I, pois na placa a superfície de contato é menor.
CORRETO. Quanto maior a superfície de contato, mais rápico ocorre a realçao
b) a quantidade de gás carbônico produzida no experimento II é menor que aquela produzida no experimento III, pois o carbonato estava despedaçado.
INCORRETO. Se a massa de carbonato é igua nos dois experimentos, então, o volume de gás produzido é o mesmo.
c) o volume de gás carbônico verificado na seringa no experimento III é menor que o volume do mesmo gás na seringa do experimento I, em função da pulverização do carbonato.
INCORRETO. Vide b)
d) o efeito do ácido sulfúrico na reação do experimento I é diferente do efeito no experimento II, produzindo uma mistura de gases, além do gás carbônico.
INCORRETO. Não há mistura de gases nesta reação, apenas a liberação de CO2, a superfície de contato altera a velocidade da reação, não os produtos.